Содержание
Особенности диеты при обострении хронического панкреатита
При обострении панкреатита диета ограничивает жиры, так как они нагружают пораженный орган и печень. Жирные продукты требуют большого количества энзимов для переваривания, что увеличивает нагрузку на больной орган. В период максимально выраженного воспалительного процесса можно добавлять в пищу только растительное масло в рафинированном виде.
Рацион при возникновении обострения
Во время обострения панкреатита основой питания является углеводно-белковая диета. Белки помогают восстановить поврежденные клетки органа. Если есть подозрение на сахарный диабет, необходимо сократить количество углеводов, особенно сладостей и простых сахаров, которые быстро усваиваются.
Во время обострения хронического панкреатита необходимо ограничить употребление соли на 15-20 дней из-за отека железы.
Еда должна быть теплой и мягкой, без добавления специй. Рекомендуется употреблять ее в небольших порциях до 8 раз в день. Это поможет избежать избыточной выработки ферментов в организме в связи с перееданием и защитит пораженный орган.
Это поможет избежать избыточной выработки ферментов в организме в связи с перееданием и защитит пораженный орган.
Список необходимых продуктов и что можно есть из блюд на первых порах, подробно объяснит врач. Существует специальная таблица, где они подробно указаны.
Каши составляют основу питания для ребенка и взрослого в стадию обострения.
Тяжелыми считаются пшенка и перловка, их не включают в рацион. Готовится блюдо на воде: цельное свежее молоко вызывает метеоризм и диарею, поэтому его исключают из меню. Из молочных продуктов можно употреблять нежирную простоквашу и кефир, а также творог с жирностью не выше 9%. Черный хлеб запрещен, но разрешается сухое галетное печенье.
Все вышеперечисленное входит в диету № 5 — она разработана для применения при панкреатите в стадии обострения. Учитывается также имеющийся сопутствующий диагноз: гастрит, желчнокаменный холецистит. Удаленный желчный пузырь часто сопутствует усилению воспаления и отека железы и требует неукоснительного соблюдения правильного питания.
При обострении или неполной ремиссии существует запрет на определенные блюда. Нельзя кушать еду в жареном, копченом и маринованном виде.
Необходимо тщательно контролировать питание ребенка.
Питье при возникновении обострения
В случае выраженного воспалительного процесса в течение первых 2-3 дней рекомендуется соблюдать голод и употреблять только жидкость. Врач назначает объем жидкости, количество приемов и объем каждой порции, учитывая тяжесть состояния пациента. Примерный объем жидкости в сутки составляет 2,5 литра.
Не стоит пить газировку, горячие или холодные напитки. Жидкость должна быть комфортной температуры, чтобы не раздражать слизистую.
Если больной может глотать, у него нет многократной рвоты, назначаются:
- щелочная минеральная вода (Боржоми, Славяновская, Смирновская, Поляна Квасова) в теплом виде без газа,
- некрепкий чай,
- компоты,
- кисели.
Часто пить небольшими глотками. Если нужно продлить питьевой режим больного более 3 дней из-за тяжелого состояния или есть любые пищеварительные проблемы, и лечение должно продолжаться в отделении интенсивной терапии, то проводится внутривенное питание раствором глюкозы с витаминами.
Список запрещенных продуктов
При выраженном обострении под запретом оказываются многие продукты. Противопоказаны:
- жирная, жареная, копченая, маринованная пища, острые приправы,
- наваристые или жирные бульоны,
- бобовые,
- овощи в свежем виде,
- колбасные продукты, консервы,
- молочные продукты,
- сдоба, мягкий белый хлеб,
- яйца,
- крепкий чай, кофе.
Следует отказаться от употребления десертов, содержащих шоколад, жирный крем и мороженое.
Примерное меню при обострении панкреатита на неделю
Если заболевание обостряется, составляется индивидуальный рацион, обеспечивающий полный функциональный покой воспаленной железе.
Полностью воздерживаться от еды рекомендуется до того времени, пока не купируется болевой синдром.
Если пациент находится в стабильном состоянии, то ему рекомендуется употреблять небольшое количество пищи в соответствии с диетой № 5П, представленной в виде кашицеобразной массы или пюре. Вечером же следует выпить стакан обезжиренного кефира. Это позволяет пациенту быстро восстановиться, так как при соблюдении диеты все признаки болезни постепенно исчезают, и наступает стадия ремиссии.
Вечером же следует выпить стакан обезжиренного кефира. Это позволяет пациенту быстро восстановиться, так как при соблюдении диеты все признаки болезни постепенно исчезают, и наступает стадия ремиссии.
Меню напоминает столы № 1а и 1б, которые рекомендуются при язвенной болезни, когда есть боли в желудке и диспептические симптомы. Отличие заключается в меньшем количестве молока и ограниченном потреблении яиц. Все блюда готовятся без добавления соли.
Первый день
- 1 завтрак — полпорции супа слизистой консистенции, половина стакана минеральной воды,
- 2 завтрак — запеченное яблоко, очищенное от кожуры,
- обед — картофель в виде несоленого пюре, без масла (половина порции), простокваша,
- ужин — пюреобразная каша из риса, слабозаваренный чай,
- перед сном — вода, сухарик.
Второй день
- 1 завтрак — омлет из белков (не больше 2), чай из ромашки,
- 2 завтрак — банан,
- обед — суп из овощей, сделанный в пароварке,
- ужин – вода, галета,
- перед сном – обезжиренный кефир.

Третий день
- 1 завтрак — овсянка с добавлением изюма, шиповниковый чай,
- 2 завтрак — кисель,
- обед — отварная рыба, кабачки, вчерашний хлеб, компот,
- ужин — паровая котлета, перетертая морковь, некрепкий чай,
- перед сном — фруктовое желе.
Четвертый день
На четвёртый день заметно улучшение состояния и постепенное расширение рациона.
- 1 завтрак — омлет из двух белков, слизистая овсянка без масла, теплый слабый несладкий чай,
- 2 завтрак — творог, нежирный кефир,
- обед — суп из гречки, говяжье рагу, чай,
- ужин — морковное пюре, куриная котлета на пару, отвар из шиповника,
- перед сном — нежирный кефир.
Пятый день
- 1 завтрак — жидкая каша из манной крупы, чай,
- 2 завтрак — желе из яблок, стакан минеральной воды без газа,
- обед — суп из овсянки, пюре из картофеля, паровая рыбная котлета, некрепкий чай,
- ужин — протертая разваренная гречневая каша на воде без масла, творожное суфле,
- перед сном — кисель.

Шестой день
- 1 завтрак — картофельное пюре, ломтик черствого хлеба или сухарик, чай,
- 2 завтрак — белковый омлет, кисель,
- обед — отварные протертые овощи с перемолотым мясом, компот,
- ужин — запеканка из нежирного творога, чай,
- перед сном — кефир.
Седьмой день
- 1 завтрак — каша из риса на воде, тщательно протертая, отварная свекла, чай из шиповника,
- 2 завтрак — желе из ягод,
- обед — слизистый суп из овсяных хлопьев, мясное суфле с пюре из моркови, чай,
- ужин — творог нежирный, галеты,
- перед сном — вода, сухарик.
Питание больного при затухании симптомов
Когда воспаление начинает стихать, и болезнь переходит в стадию ремиссии, меню расширяется, включаются новые продукты. В этот период назначается протертый вариант диеты № 5Б. Она применяется для предотвращения рецидивов и прогрессирования болезни, для коррекции возникающих погрешностей в питании. Для снижения функциональной нагрузки на железу в приготовлении блюд, соответствующих столу № 5Б, применяется обработка:
Механическое действие продуктов зависит от нескольких показателей:
- степени измельчения,
- консистенции пищи,
- употребляемого однократного объема порции,
- характера обработки пищи (варка, приготовление на пару, тушение).

Химическое воздействие оценивается качеством еды: категорически запрещены экстрактивные вещества и эфирные масла. Это самые сильные раздражители органов пищеварения, вызывают выработку большого количества желудочного и панкреатического сока.
Минимальное воздействие термического фактора наблюдается, когда температура употребляемых блюд приближена к температуре тела.
Когда все симптомы заболевания и боли пропадают, пациенту рекомендуется следовать диете № 5Б без измельчения продуктов. Если болезнь находится в стабильной ремиссии, не требуется строгое механическое измельчение пищи.
При уменьшении симптомов болезни диетические принципы остаются неизменными — ограничения в качестве и количестве потребляемой пищи.
Высокое количество белка, но уменьшение жира и простых углеводов:
- белок — 100–120 грамм в сутки, при выраженном снижении веса больного — 130 грамм в сутки,
- жиры — 70 грамм в сутки (нижняя граница допустимой нормы), из них 20% – должны быть растительные,
- углеводы — 350–400 г, ограничение простых углеводов до 30 грамм в сутки.

Калорийность составляет 2500 ккал, необходимо выпивать 1500 мл жидкости в день, ограниченное количество соли — 6-8 грамм в день.
В течение 14 дней после обострения следует приготавливать блюда путем варки или парения, измельчать или протирать. Рекомендуется варить мясо порциями в 100 г, сливая первый бульон, что может привести к потере до 65% экстрактивных веществ.
Из круп предпочтительнее рис, гречка, овсянка (хлопья). После проваривания их перетирают до полувязкого состояния.
- яйцо всмятку 1 раз в день или белковый омлет,
- отварные овощи в перетертом виде, небольшое количество свежих при нормальной переносимости,
- печеные яблоки, желе, варенье на ксилите,
- сливочное масло до 20 г в день и рафинированное подсолнечное до 5–15 мл – вводить рекомендуется постепенно, начиная с минимального количества.
- маринованные и жареные блюда, копчености, острые приправы,
- рассыпчатые каши,
- ржаной и белый свежевыпеченный хлеб, сдобу,
- супы на крепких мясных бульонах,
- кофе, мороженое, мед, шоколад, варенье, сок из винограда.

Диетическое питание имеет хороший отзыв от пациентов: удается значительно сократить список и дозы принимаемых медикаментов и улучшить общее состояние.
Панкреатит — заболевание, которое может вернуться и продолжаться. Поэтому соблюдение диеты во время обострения является важным и необходимым для лечения. Нарушение здорового питания может привести к ухудшению функций поджелудочной железы и постоянной необходимости соблюдать диету.
Питание при панкреатите в период обострения:
При обострении панкреатита следует воздержаться от еды на несколько дней. Во время голодания рекомендуется пить только очищенную негазированную воду. Дневной объем воды не должен превышать 1,5-1,7 литра. После уменьшения болевых ощущений и симптомов можно добавлять в рацион небольшое количество низкокалорийной пищи, такой как жидкие каши, овощные супы, паровые котлеты из рыбы или куриного мяса.
Питание при хроническом панкреатите:
При хроническом панкреатите необходимо строго следить за рационом. Соблюдение правильного режима питания помогает предотвратить обострения. Каждое обострение ухудшает функцию железы.
Соблюдение правильного режима питания помогает предотвратить обострения. Каждое обострение ухудшает функцию железы.
При длительном панкреатите требуется придерживаться питания по диете № 5.
Дробное питание до 6 раз в сутки
- количество соли не более 6 грамм
- отварные блюда в протертом или измельченном виде
- питание с повышенным содержанием белка
Меню питания при панкреатите. Режим питания
- При панкреатите следует употреблять небольшие порции пищи, приготовленной на пару или отваренной и измельченной.
- Продукты должны быть высокого качества, без добавления консервантов и красителей.
Следование правильному режиму питания и диетическим правилам поможет избежать осложнений и ухудшения состояния заболевания.
Рецепты диетических блюд при панкреатите:
Примерное меню диеты при панкреатите:
- Завтрак: гречневая каша сваренная на воде с добавлением нежирного молока. Отвар шиповника.
- Второй завтрак: запеченое яблоко.
 Травяной чай
Травяной чай - Обед: овощной суп с куриными фрикадельками. Паштет из телятины. Компот из сухофруктов
- Полдник: творожная запеканка из нежирного творога. Кисель
- Ужин: Паровая рыбная котлета с отварными овощами и рисом. Травяной чай
- Перед сном: компот из шиповника.
Диагностика хронического панкреатита
- Общий анализ крови.
- Общий анализ мочи.
- Анализ крови на биохимическое содержание амилазы, липазы и эластазы в сыворотке.
- Копрограмма.
- Определение уровня глюкозы в крови или анализ крови на содержание сахара в биохимической лаборатории.
- УЗИ органов брюшной полости.
- МРТ или КТ поджелудочной железы.
- Ангиография.
- ФГДС.
Что едят при обострении панкреатита?
В первые два дня острой фазы панкреатита больному нужно воздержаться от приема любой пищи. После этого в рацион постепенно вводятся:
- протертые крупяные супы на воде либо отваре овощей;
- паровые котлеты, нежирное отварное мясо;
- полувязкие каши;
- омлет, яйца всмятку;
- паровые творожные пудинги;
- овощное пюре;
- кисели и компоты.

Чтобы отрегулировать механизм пищеварения, в дальнейшем важно употреблять продукты, богатые витаминами A, В, C, биофлавоноидами. Для уменьшения проницаемости стенок сосудов и их укрепления следует включить в рацион пищу, насыщенную кальцием. Соблюдается диета при обострении панкреатита до полного исчезновения симптомов заболевания.
Диета при панкреатите: составляем примерное меню
Поджелудочная железа поражается серьезным воспалительным заболеванием, которое называется панкреатит. Это может быть вызвано различными причинами, такими как закупорка панкреатического протока, сосудистые расстройства, травмы, токсические отравления и даже паразитарные заболевания. Специальная диета играет важную роль в лечении панкреатита, в дополнение к медикаментозным и хирургическим методам.
Симптомы острого панкреатита
Симптомы острого панкреатита меняются в зависимости от формы заболевания – легкой или тяжелой. Легкая форма характеризуется умеренной болью и низким риском осложнений. Тяжелая форма может привести к гибели тканей поджелудочной железы, образованию абсцессов и гнойному панкреатиту.
Тяжелая форма может привести к гибели тканей поджелудочной железы, образованию абсцессов и гнойному панкреатиту.
Основные симптомы острого панкреатита1:
- тошнота и рвота, в рвотных массах иногда присутствует желчь;
- выраженная боль в левом подреберье;
- высокая температура;
- жидкий стул;
- скачки артериального давления;
- вздутие живота, тяжесть;
- появление кровоизлияний в пупочной области.
При остром воспалении поджелудочной железы нарушается отток панкреатического сока, что вызывает переваривание тканей железы и появление сильной опоясывающей боли. Боль возникает внезапно после переедания, употребления жирной пищи или алкоголя.
При остром панкреатите возможно начало болевого приступа вместе с увеличением артериального давления. Однако может произойти обратное — давление внезапно снижается, пациент становится бледным, чувствует сильную слабость, начинает потеть. Эти признаки могут указывать на развитие шока, требующего немедленной медицинской помощи.
Причины острого панкреатита
Панкреатит может быть инфекционным или неинфекционным. В случае вирусного панкреатита, поджелудочная железа поражается инфекцией, например, при кори, вирусном гепатите или туберкулезе.
Диагностика острого панкреатита
При остром панкреатите проводят обследование, которое назначает гастроэнтеролог или хирург. Важно провести лабораторные и инструментальные методы диагностики вовремя, чтобы получить максимально полную информацию о состоянии поджелудочной железы и сопутствующих органов. Симптомы острого панкреатита могут быть похожи на клинические проявления других заболеваний (аппендицит, холецистит), что может привести к неправильному выбору тактики лечения.
Лечение хронического панкреатита в СПб
Лечение хронического панкреатита (ХП), как и любого другого хронического заболевания, направлено на снятие или уменьшение беспокоящих человека симптомов и улучшение качества его жизни. Для этого, в первую очередь, необходимо убрать болевой синдром, снять спазм сфинктера печеночно-поджелудочной ампулы и улучшить отток панкреатического сока и желчи.
Необходимо добиться улучшения процесса пищеварения, компенсировать уже имеющуюся секреторную недостаточность поджелудочной железы. И в третьих, остановить дальнейшее прогрессирование заболевания. И с этой целью исключить те факторы, которые явились причиной развития ХП, подавить воспалительные и дегенеративные процессы в поджелудочной железе, и проводить профилактику обострений ХП, используя диету, санаторно-курортное лечение и реабилитацию.
Лечебная программа при хроническом панкреатите включает:
1. Устранение причин, вызывающих болезнь. Необходимо полностью исключить употребление алкоголя, прекратить употребление веществ, которые могут оказывать повреждающее действие на ткань поджелудочной железы. Если речь идет о лекарственных препаратах, по возможности нужно снизить прием или вместе с лечащим врачом подобрать замену. Пройти медикаментозное лечение тех заболеваний желудка, двенадцатиперстной кишки, гепатобилиарной зоны, которые могут негативно отражаться на функции поджелудочной железы.
2. Устранение боли. С этой целью используют не только обезболивающие, но и медикаменты, снимающие спазм (спазмолитики). При этом нужно помнить, что при приеме обезболивающих лекарств в течение длительного времени может возникнуть привыкание, зависимость от приема анальгетиков. Наркотические анальгетики могут применяться только для снятия очень сильного болевого синдрома, нечувствительного к другим обезболивающим средствам. У некоторых больных сильную боль удается купировать только в стационаре, выполнив новокаиновую блокаду. Также для уменьшения боли следует принимать препараты, снимающие спазм сфинктера фатерова соска, восстанавливающие отток панкреатического сока и, в результате, приводящие к снижению давления в протоках железы, а также лекарства, уменьшающие дискинезию желудочно-кишечного тракта.
3. Купирование обострений хронического панкреатита. Подавление процесса «самопереваривания» поджелудочной железы, снятие интоксикации, устранение обменных нарушений, профилактику полиорганной недостаточности. В этом процессе важным мероприятием является подавление секреции поджелудочной железы. В настоящее время для этого применяется сандостатин или октреотид (аналоги соматостатина).
В этом процессе важным мероприятием является подавление секреции поджелудочной железы. В настоящее время для этого применяется сандостатин или октреотид (аналоги соматостатина).
4. Профилактика обострений включает соблюдение диеты и режима питания, санаторно-курортное лечение и реабилитацию. При обострении заболевания разрешается щелочная минеральная вода, чай, отвар из шиповника, белковые омлеты на пару. Количество выпиваемой жидкости должно быть достаточным для обеспечения потребностей организма (1,5- 2, даже 2,5 литра с сутки). В последующем можно есть вегетарианские супы или супы-пюре, кисели, картофельное и морковное пюре, жидкие каши на воде с ограничением животных жиров. По мере того, как проходят диспептические явления и уменьшаются боли, рацион можно разнообразить: можно есть белые сухари, мясные блюда из варенного или приготовленного на пару мяса, отварную нежирную рыбу, обезжиренный творог, крупяные пудинги.
Нужно помнить, что даже после купирования приступа и исчезновения болей соблюдение диеты является обязательным. При наличии хронического панкреатита употребление в пищу жира должно быть уменьшено до 70-80 г в сутки, в основном следует использовать растительные масла, которые легко эмульгируются и хорошо всасываются.
При наличии хронического панкреатита употребление в пищу жира должно быть уменьшено до 70-80 г в сутки, в основном следует использовать растительные масла, которые легко эмульгируются и хорошо всасываются.
Хорошо переносится пища, обогащенная белком (до 110-120 г/сут). Предпочтение следует отдать молочным продуктам, приготовленным из обезжиренного молока, в частности нежирному свежему творогу. Можно есть нежирное отварное мясо, нежирную рыбу также отварную или приготовленную на пару. Можно есть свежие фрукты, овощные супы, супы-пюре, овощные пюре или пудинги, соки. Ни в коем случае нельзя есть продукты, стимулирующие работу поджелудочной железы: острые приправы, копчености, мясные и рыбные консервы. В целом пищевой рацион постоянно должен быть близок к диете N 5.
Употребление алкоголя категорически запрещается. Из рациона исключают тугоплавкие жиры, холодные шипучие напитки, свежий теплый хлеб.
Для покрытия энергетических расходов и восстановления массы тела дополнительно к диетической пище добавляют специальные питательные смеси. Особенно полезны смеси для энтерального питания, обогащенные витаминами и необходимыми микроэлементами.
Особенно полезны смеси для энтерального питания, обогащенные витаминами и необходимыми микроэлементами.
5. Коррекция внешне- и внутрисекреторной недостаточности поджелудочной железы. При наличии явной внутрисекреторной недостаточности поджелудочной железы (развитии панкреатогенного сахарного диабета) необходимо корректировать нарушения углеводного обмена. То есть необходимо соблюдать диету, контролировать уровень сахара в крови и, при необходимости, по назначению эндокринолога, принимать снижающие сахар препараты или использовать инсулин. Больным ХП, который протекает с проявлениями внешнесекреторной недостаточности (нехватки ферментов для нормального переваривания пищи) и нарушения процесса пищеварения, особенно при явлениях мальдигестии, мальабсорбции и стеатореи, назначают заместительную терапию препаратами, содержащими ферменты поджелудочной железы. Принято считать, что заместительная ферментная терапия абсолютно необходима, если ежедневное выведение жира превышает 15 г и у больного постоянно уменьшается масса тела.
6. Нормализация деятельности пищеварительной системы. При лечении ХП важное значение имеет нормализация функций всего пищеварительного тракта, печени и желчевыводящих путей, так как это замедляет прогрессирование болезни, уменьшает частоту обострений. Под контролем гастроэнтеролога проводят лечение гастрита, дуоденита, рефлюксной болезни. При дисбактериозе кишечника, осложнившем течение ХП, принимают антибиотики, подавляющие патогенную кишечную флору, а затем препараты содержащие нормальную кишечную флору.
При нарушении функции печени назначают гепатопротекторы. Случаев полного излечения ХП не описано, однако значительное улучшение под влиянием систематических лечебных мероприятий и возникновение стойкой ремиссии на протяжении 5 лет и более возможно у большинства больных.
Эндоскопические методы лечения при хроническом панкреатите
Начиная с середины 70-х годов XX века, начали успешно применять эндоскопические технологии для лечения больных ХП. Эндоскопические вмешательства при ХП направлены, в первую очередь, на облегчение боли путем устранения протоковой панкреатической гипертензии, напряженных кистозных образований.
Эндоскопические вмешательства при ХП направлены, в первую очередь, на облегчение боли путем устранения протоковой панкреатической гипертензии, напряженных кистозных образований.
Показания для выполнения эндоскопических вмешательств при хроническом панкреатите:
- сдавление общего желчного протока увеличенной плотной головкой поджелудочной железы (дистальный стеноз холедоха) с нарушением оттока желчи и развитием желтухи;
- стеноз большого дуоденального соска (папиллостеноз), его рубцовое сужение; множественные и одиночные камни в главном протоке поджелудочной железы;
- свищи поджелудочной железы, связанные с главным протоком железы;
- кисты или псевдокисты, расположенные вблизи двенадцатиперстной кишки или желудка, оказывающие давление или выпячивающие стенку органа.
Такое вмешательство может включать:
- рассечение большого дуоденального сосочка (БДС) и сфинктера (папиллосфинктеротомию) главного или добавочного протоков поджелудочной железы,
- установку временного назопанкреатического дренажа, эндопротеза (стента) в проток через место его сужения,
- удаление панкреатических камней.
 Удалению конкрементов может способствовать лазерная или контактная литотрипсия в сочетании со сфинктеротомией и эндоскопической экстракцией разрушенных конкрементов.
Удалению конкрементов может способствовать лазерная или контактная литотрипсия в сочетании со сфинктеротомией и эндоскопической экстракцией разрушенных конкрементов.
Клинический эффект (существенное уменьшение или исчезновение боли) при дренировании протока поджелудочной железы отмечается у большинства успешно (в техническом отношении) прооперированных пациентов. Эти дает возможность отказаться после вмешательства от приема анальгетиков, позволяет избежать тяжелых обострений ХП, улучшается функция поджелудочной железы, улучшается пищеварение. Повышается масса тела. Подобный клинический эффект имеет обычно временный характер, через 2 года примерно у 27% больных наступает рецидив боли. Если на фоне хронического панкреатита формируются псевдокисты также возможно выполнить малоинвазивные операции, такие как чрескожное дренирование или эндоскопический внутренний дренаж.
Основная цель этих операций — создание сообщения между просветом псевдокисты и просветом желудка или кишечника, для обеспечения оттока панкреатического сока. Подобное соустье между кистой и желудком может быть выполнено только в том случае, если стенка кисты и стенка желудка тесно прилегают.
Подобное соустье между кистой и желудком может быть выполнено только в том случае, если стенка кисты и стенка желудка тесно прилегают.
Хирургическое лечение при хроническом панкреатите
Главная цель хирургического лечения при ХП устранение абдоминального болевого синдрома и максимальное сохранение экзокринной и эндокринной функции поджелудочной железы.
Показаниями к хирургическому вмешательству при ХП являются:
- кальциноз поджелудочной железы и камни протоков с выраженным болевым синдромом;
- нарушение проходимости и значительное расширение протока поджелудочной железы;
- возникновение обтурационной желтухи и холангита за счет сдавления общего желчного протока;
- сдавление и нарушение проходимости двенадцатиперстной кишки;
- сегментарная портальная гипертензия за счет сдавления и тромбоза вен бассейна воротной вены;
- формирование кисты более 6 см в диаметре или свища поджелудочной железы, не излечивающихся консервативными методами в течение 3 мес;
- вторичный ХП, обусловленный желчнокаменной болезнью, пенетрирующей гастродуоденальной язвой, дуоденостазом, абдоминально-ишемическим синдромом;
- сильный болевой синдром и похудение с частыми рецидивами панкреатита при отсутствии эффекта от консервативного лечения; невозможность до операции исключить наличие злокачественной опухоли.

Выполняют операции как на самой на поджелудочной железе, так и на вегетативной нервной системе, желчных путях, желудке и других органах брюшной полости.
Выбор способа операции зависит от степени тяжести морфологических нарушений, как в самой поджелудочной железе, так и в смежных органах.
- Дренирующие хирургические операции на поджелудочной железе показаны в случаях расширения и деформации ее главного протока, вирсунголитиаза. Они включают рассечение и пластику устья главного протока поджелудочной железы, внутреннее дренирование протоков железы, окклюзию протоков.
- Резекции поджелудочной железы при хроническом панкреатите выполняют при псевдотуморозном варианте хронического панкреатита, в случаях, когда имеется подозрение на опухолевый процесс в железе.
- Операции на желчных путях у больных ХП применяют при сопутствующей желчнокаменной болезни, стенозе общего желчного протока или большого сосочка двенадцатиперстной кишки, развитии холестаза или механической желтухи.
 Может быть выполнена холецистэктомия (как традиционая, так и лапароскопическая) с дренированием общего желчного протока, или наложен билиодигестивный анастомоз (сформировано сообщение между желчным протоком и кишкой -двенадцатиперстной или тощей), выполнена папиллосфинктеротомия(рассечение рубцово суженого большого дуоденального соска) или папиллосфинктеропластика.
Может быть выполнена холецистэктомия (как традиционая, так и лапароскопическая) с дренированием общего желчного протока, или наложен билиодигестивный анастомоз (сформировано сообщение между желчным протоком и кишкой -двенадцатиперстной или тощей), выполнена папиллосфинктеротомия(рассечение рубцово суженого большого дуоденального соска) или папиллосфинктеропластика. - Операции на сосудах: чревном стволе и верхней брыжеечной артерии выполняют при ишемическом поражении поджелудочной железы. Ишемия может возникнуть вследствие артериосклеротического поражения, реже сдавления диафрагмой чревного ствола, врожденного сужения и атрезии, мышечно-соединительнотканной гиперплазии стенки сосуда, артериита, спаек, перекрута артерий и др. В этих случаях выполняют декомпрессию чревного ствола как традиционным, так и лапароскопическим способом, тромбэндартерэктомию, пластику артерии или другие сосудистые вмешательства.
- Операции на вегетативной нервной системе производят при выраженном болевом синдроме, если другие способы лечения оказались неэффективны.
 Они направлены на купирование боли и снижение функции поджелудочной железы.
Они направлены на купирование боли и снижение функции поджелудочной железы.
Строго дифференцированный подход к выбору метода лечения, способа и объема хирургического вмешательства является одним из основных факторов улучшения результатов лечения больных хроническим панкреатитом. В нашем Центре хирурги имеют большой опыт лечения пациентов, страдающих хроническим панкреатитом.
Лечение боли при хроническом панкреатите с упором на экзогенные ферменты поджелудочной железы
1. Howard JM, Hess W. New York: Kluwer Adademic/Plenum Publishers; 2002. История поджелудочной железы: Тайны скрытого органа. [Google Scholar]
2. Cawley T. Один случай диабета, полностью связанный с качеством мочи, с исследованием различных теорий этого заболевания. London Med J. 1788; 9: 286–301. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Johnston GW. Калькулезные и другие поражения протоков поджелудочной железы. Am J Med Sci. 1883; 86: 404–429. . [Google Scholar]
. [Google Scholar]
4. Сингер М.В., Гир К., Сарлес Х. Пересмотренная классификация панкреатита. Отчет Второго международного симпозиума по классификации панкреатита в Марселе, Франция, 28-30 марта 1984 г. Гастроэнтерология. 1985; 89: 683–685. [PubMed] [Google Scholar]
5. Сарнер М., Коттон П.Б. Классификация панкреатита. Кишка. 1984; 25: 756–759. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Steer ML, Waxman I, Freedman S. Хронический панкреатит. N Engl J Med. 1995;332:1482–1490. [PubMed] [Google Scholar]
7. Гупта В., Тоскес П.П. Диагностика и лечение хронического панкреатита. Postgrad Med J. 2005; 81: 491–497. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Афгани Э., Синха А., Сингх В.К. Обзор диагностики и управления питанием при хроническом панкреатите. Нутр Клин Практ. 2014;29:295–311. [PubMed] [Google Scholar]
9. Хаякава Т., Кондо Т., Шибата Т., Нода А., Судзуки Т., Накано С. Связь между экзокринной функцией поджелудочной железы и гистологическими изменениями при хроническом панкреатите. Am J Гастроэнтерол. 1992;87:1170–1174. [PubMed] [Google Scholar]
Am J Гастроэнтерол. 1992;87:1170–1174. [PubMed] [Google Scholar]
10. Чоудхури Р.С., Forsmark CE. Обзорная статья: Тестирование функции поджелудочной железы. Алимент Фармакол Тер. 2003; 17: 733–750. [PubMed] [Google Scholar]
11. Каталано М.Ф., Сахаи А., Леви М., Романьоло Дж., Вирсема М., Брюгге В., Фриман М., Ямао К., Канто М., Эрнандес Л.В. Основанные на ЭУЗИ критерии диагностики хронического панкреатита: классификация Роузмонта. Гастроинтест Эндоск. 2009;69:1251–1261. [PubMed] [Google Scholar]
12. Yadav D, Hawes RH, Brand RE, Anderson MA, Money ME, Banks PA, Bishop MD, Baillie J, Sherman S, DiSario J, et al. Употребление алкоголя, курение сигарет и риск рецидивирующего острого и хронического панкреатита. Arch Intern Med. 2009 г.;169:1035–1045. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Pitchumoni CS. Хронический панкреатит: патогенез и лечение боли. Дж. Клин Гастроэнтерол. 1998; 27:101–107. [PubMed] [Google Scholar]
14. Layer P, Yamamoto H, Kalthoff L, Clain JE, Bakken LJ, DiMagno EP. Различное течение раннего и позднего идиопатического и алкогольного хронического панкреатита. Гастроэнтерология. 1994; 107:1481–1487. [PubMed] [Google Scholar]
Различное течение раннего и позднего идиопатического и алкогольного хронического панкреатита. Гастроэнтерология. 1994; 107:1481–1487. [PubMed] [Google Scholar]
15. Braganza JM, Lee SH, McCloy RF, McMahon MJ. Хронический панкреатит. Ланцет. 2011; 377:1184–1197. [PubMed] [Google Scholar]
16. DiMagno EP, Layer P, Clain JE. Нью-Йорк: Рейвен Пресс; 1993. Хронический панкреатит. В: VLWGo, редактор. Поджелудочная железа: биология, патобиология и болезнь. 2-е изд.; стр. 665–706. [Google Scholar]
17. Lankisch PG, Löhr-Happe A, Otto J, Creutzfeldt W. Естественное течение хронического панкреатита. Боль, экзокринная и эндокринная недостаточность поджелудочной железы и прогноз заболевания. пищеварение. 1993; 54: 148–155. [PubMed] [Google Scholar]
18. Pitchumoni CS. Алкоголь при хроническом панкреатите. Это провоцирует боль? Дж. Клин Гастроэнтерол. 1995;20:4–5. [PubMed] [Google Scholar]
19. Ammann RW, Akovbiantz A, Largiader F, Schueler G. Течение и исход хронического панкреатита. Продольное исследование смешанной медико-хирургической серии 245 пациентов. Гастроэнтерология. 1984; 86: 820–828. [PubMed] [Google Scholar]
Продольное исследование смешанной медико-хирургической серии 245 пациентов. Гастроэнтерология. 1984; 86: 820–828. [PubMed] [Google Scholar]
20. Ammann RW, Muellhaupt B. Естественная история боли при алкогольном хроническом панкреатите. Гастроэнтерология. 1999;116:1132–1140. [PubMed] [Google Scholar]
21. Гирдвуд А.Х., Маркс И.Н., Борнман П.С., Коттлер Р.Э., Коэн М. Ограничивает ли прогрессирующая панкреатическая недостаточность боль при кальцифицирующем панкреатите со стриктурой протока или продолжающимся алкогольным отравлением? Дж. Клин Гастроэнтерол. 1981;3:241–245. [PubMed] [Google Scholar]
22. Enweluzo C, Tlhabano L. Лечение боли при хроническом панкреатите: приручение зверя. Клин Эксп Гастроэнтерол. 2013; 6: 167–171. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Levrat M, Descos L, Moulinier B, Pasquier J. [Длительное развитие хронического панкреатита (113 случаев). II. Изучение течения хронического панкреатита у оперированных больных] Arch Fr Mal App Dig. 1970; 59: 305–314. [PubMed] [Google Scholar]
1970; 59: 305–314. [PubMed] [Google Scholar]
24. Mullady DK, Yadav D, Amann ST, O’Connell MR, Barmada MM, Elta GH, Scheiman JM, Wamsteker EJ, Chey WD, Korneffel ML, et al. Тип боли, осложнения, связанные с болью, качество жизни, инвалидность и использование ресурсов при хроническом панкреатите: проспективное когортное исследование. Кишка. 2011;60:77–84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Warshaw AL, Banks PA, Fernández-Del Castillo C. Технический обзор AGA: лечение боли при хроническом панкреатите. Гастроэнтерология. 1998; 115: 765–776. [PubMed] [Google Scholar]
26. Каранджия Н.Д., Ребер Х.А. Причины и лечение боли при хроническом панкреатите. Гастроэнтерол Клин Норт Ам. 1990; 19: 895–904. [PubMed] [Google Scholar]
27. Гачаго С., Драганов П.В. Лечение боли при хроническом панкреатите. Мир J Гастроэнтерол. 2008; 14:3137–3148. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Сакорафас Г.Х., Циотоу А.Г., Перос Г. Механизмы и естественное течение боли при хроническом панкреатите: хирургическая перспектива. Дж. Клин Гастроэнтерол. 2007; 41: 689–699. [PubMed] [Google Scholar]
Дж. Клин Гастроэнтерол. 2007; 41: 689–699. [PubMed] [Google Scholar]
29. Брэдли Э.Л. Давление в протоке поджелудочной железы при хроническом панкреатите. Am J Surg. 1982; 144: 313–316. [PubMed] [Google Scholar]
30. Мэдсен П., Винклер К. Внутрипротоковое давление поджелудочной железы при хроническом обструктивном панкреатите. Scand J Гастроэнтерол. 1982; 17: 553–554. [PubMed] [Академия Google]
31. Ebbehøj N, Borly L, Bülow J, Rasmussen SG, Madsen P. Оценка давления жидкости в тканях поджелудочной железы и боли при хроническом панкреатите. Продольное исследование. Scand J Гастроэнтерол. 1990; 25: 462–466. [PubMed] [Google Scholar]
32. Mössner J. Смягчение боли при хроническом панкреатите. Использование ферментов. Surg Clin North Am. 1999;79:861–872, xi. [PubMed] [Google Scholar]
33. Ebbehøj N, Borly L, Bülow J, Rasmussen SG, Madsen P, Matzen P, Owre A. Давление жидкости в тканях поджелудочной железы при хроническом панкреатите. Отношение к боли, морфологии и функции. Scand J Гастроэнтерол. 1990;25:1046–1051. [PubMed] [Google Scholar]
Scand J Гастроэнтерол. 1990;25:1046–1051. [PubMed] [Google Scholar]
34. Каранджиа Н.Д., Сингх С.М., Уиддисон А.Л., Лутрин Ф.Дж., Ребер Х.А. Протоковое и интерстициальное давление поджелудочной железы у кошек с хроническим панкреатитом. Dig Dis Sci. 1992; 37: 268–273. [PubMed] [Google Scholar]
35. Reber HA, Karanjia ND, Alvarez C, Widdison AL, Leung FW, Ashley SW, Lutrin FJ. Панкреатический кровоток у кошек с хроническим панкреатитом. Гастроэнтерология. 1992; 103: 652–659. [PubMed] [Google Scholar]
36. Widdison AL, Alvarez C, Schwarz M, Reber HA. Влияние этанола на панкреатический кровоток у кошек с хроническим панкреатитом. Операция. 1992;112:202–208. [PubMed] [Google Scholar]
37. Widdison AL, Karanjia ND, Reber HA. Регуляция сосудов поджелудочной железы при хроническом панкреатите у кошек. Кишка. 1995; 36: 133–136. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Тояма М.Т., Патель А.Г., Нгуен Т., Эшли С.В., Ребер Х.А. Влияние этанола на интерстициальный рН поджелудочной железы и кровоток у кошек с хроническим панкреатитом. Энн Сург. 1997; 225: 223–228. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Энн Сург. 1997; 225: 223–228. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Fasanella KE, Davis B, Lyons J, Chen Z, Lee KK, Slivka A, Whitcomb DC. Боль при хроническом панкреатите и раке поджелудочной железы. Гастроэнтерол Клин Норт Ам. 2007; 36: 335–364, ix. [PubMed] [Академия Google]
40. Кейт Р.Г., Кешавджи С.Х., Кереньи Н.Р. Нейропатология хронического панкреатита у человека. Может J Surg. 1985; 28: 207–211. [PubMed] [Google Scholar]
41. Ахмед Али У., Палплатц Дж. М., Нилон У. Х., Ван Гоор Х., Гусен Х. Г., Бурмистер М. А. Эндоскопическое или хирургическое вмешательство при болезненном обструктивном хроническом панкреатите. Cochrane Database Syst Rev. 2015;(3):CD007884. [PubMed] [Google Scholar]
42. Древес А.М., Краруп А.Л., Детлефсен С., Мальмстрем М.Л., Димцевски Г., Фунч-Йенсен П. Боль при хроническом панкреатите: роль нейропатических механизмов боли. Кишка. 2008; 57: 1616–1627. [PubMed] [Академия Google]
43. Димцевски Г., Штаал С.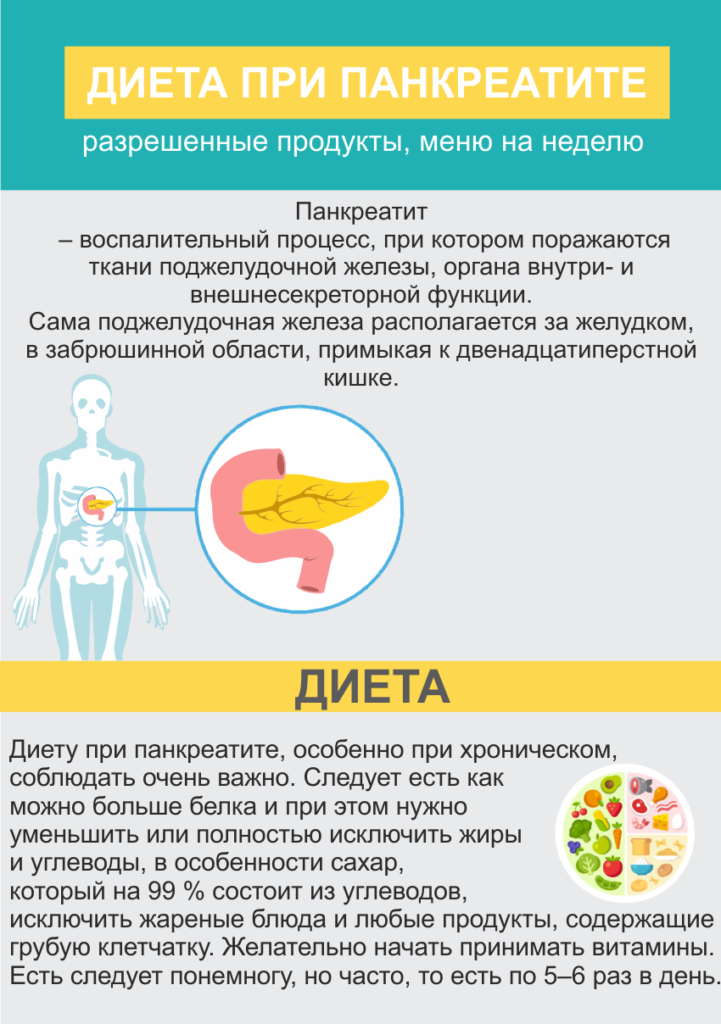 , Андерсен С.Д., Торсгаард Н., Фунч-Йенсен П., Арендт-Нильсен Л., Древес А.М. Оценка экспериментальной боли со стороны кожи, мышц и пищевода у больных хроническим панкреатитом. Поджелудочная железа. 2007; 35:22–29. [PubMed] [Google Scholar]
, Андерсен С.Д., Торсгаард Н., Фунч-Йенсен П., Арендт-Нильсен Л., Древес А.М. Оценка экспериментальной боли со стороны кожи, мышц и пищевода у больных хроническим панкреатитом. Поджелудочная железа. 2007; 35:22–29. [PubMed] [Google Scholar]
44. Димцевски Г., Сами С.А., Фунч-Йенсен П., Ле Пера Д., Валериани М., Арендт-Нильсен Л., Древес А.М. Боль при хроническом панкреатите: роль перестройки в центральной нервной системе. Гастроэнтерология. 2007; 132:1546–1556. [PubMed] [Академия Google]
45. Андрен-Сандберг А., Ансорж С., Эйрикссон К., Гломсакер Т., Малецкас А. Лечение псевдокист поджелудочной железы. Scand J Surg. 2005; 94: 165–175. [PubMed] [Google Scholar]
46. Rosso E, Alexakis N, Ghaneh P, Lombard M, Smart HL, Evans J, Neoptolemos JP. Псевдокиста поджелудочной железы при хроническом панкреатите: эндоскопическое и хирургическое лечение. Копать сург. 2003; 20: 397–406. [PubMed] [Google Scholar]
47. Домингес-Муньос Дж. Э. Экзокринная недостаточность поджелудочной железы: диагностика и лечение. J Гастроэнтерол Гепатол. 2011; 26 Дополнение 2:12–16. [PubMed] [Академия Google]
J Гастроэнтерол Гепатол. 2011; 26 Дополнение 2:12–16. [PubMed] [Академия Google]
48. Whitcomb DC, Lehman GA, Vasileva G, Malecka-Panas E, Gubergrits N, Shen Y, Sander-Struckmeier S, Caras S. Капсулы с отсроченным высвобождением панкрелипазы (CREON) для экзокринной недостаточности поджелудочной железы вследствие хронического панкреатита или панкреатита. хирургия: двойное слепое рандомизированное исследование. Am J Гастроэнтерол. 2010;105:2276–2286. [PubMed] [Google Scholar]
49. Мосснер Дж. Лечение боли при хроническом панкреатите ферментами поджелудочной железы. Другая точка зрения. Ферменты поджелудочной железы в норме и при патологии. В: Lankisch PG, редактор. Берлин: Springer-Verlag; 1991. стр. 103–112. [Google Scholar]
50. Струм В.Б. Абстиненция при алкогольном хроническом панкреатите. Влияние на боль и результат. Дж. Клин Гастроэнтерол. 1995; 20:37–41. [PubMed] [Google Scholar]
51. Domínguez-Muñoz JE, Iglesias-García J. Пероральная заместительная терапия ферментами поджелудочной железы при хроническом панкреатите: является ли клинический ответ подходящим маркером для оценки терапевтической эффективности? JOP. 2010; 11: 158–162. [PubMed] [Google Scholar]
2010; 11: 158–162. [PubMed] [Google Scholar]
52. Бхардвадж П., Тареджа С., Пракаш С., Сарая А. Потребление микронутриентов-антиоксидантов у пациентов с хроническим панкреатитом. Троп Гастроэнтерол. 2004;25:69–72. [PubMed] [Google Scholar]
53. Lindkvist B, Domínguez-Muñoz JE, Luaces-Regueira M, Castiñeiras-Alvariño M, Nieto-Garcia L, Iglesias-Garcia J. Питательные маркеры сыворотки для прогнозирования экзокринной недостаточности поджелудочной железы при хронических панкреатит. Панкреатология. 2012;12:305–310. [PubMed] [Google Scholar]
54. Каваллини Г., Таламини Г., Ваона Б., Бово П., Филиппини М., Риго Л., Анджелини Г., Вантини И., Риела А., Фруллони Л. Влияние алкоголя и курения на литогенез поджелудочной железы у течение хронического панкреатита. Поджелудочная железа. 1994;9:42–46. [PubMed] [Google Scholar]
55. Роуз П., Фрейн Э., Хант Л.П., Ачесон Д.В., Браганза Дж.М. Пищевые антиоксиданты и хронический панкреатит. Хум Нутр Клин Нутр. 1986; 40: 151–164. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
56. Bowrey DJ, Morris-Stiff GJ, Puntis MC. Дефицит селена и хронический панкреатит: механизм заболевания и потенциал терапии. HPB Surg. 1999;11:207–215; обсуждение 215-216. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Бэнкс П.А., Хьюз М., Ферранте М., Нордхук Э.К., Рамагопал В., Сливка А. Уменьшает ли аллопуринол боль при хроническом панкреатите? Int J Панкреатол. 1997;22:171–176. [PubMed] [Google Scholar]
58. Бхардвадж П., Гарг П.К., Маулик С.К., Сарая А., Тандон Р.К., Ачарья С.К. Рандомизированное контролируемое исследование антиоксидантных добавок для облегчения боли у пациентов с хроническим панкреатитом. Гастроэнтерология. 2009;136:149–159.e2. [PubMed] [Google Scholar]
59. Вольф Г., Мюллер Г. М., Керберг Г. [Влияние карбоната лития на количество лейкоцитов после ионизирующего облучения. 4. Влияние карбоната лития на активацию гранулоцитов] Radiobiol Radiother (Berl) 1989;30:546–552. [PubMed] [Google Scholar]
60. Morris-Stiff GJ, Bowrey DJ, Oleesky D, Davies M, Clark GW, Puntis MC. Антиоксидантный профиль больных рецидивирующим острым и хроническим панкреатитом. Am J Гастроэнтерол. 1999;94:2135–2140. [PubMed] [Google Scholar]
Morris-Stiff GJ, Bowrey DJ, Oleesky D, Davies M, Clark GW, Puntis MC. Антиоксидантный профиль больных рецидивирующим острым и хроническим панкреатитом. Am J Гастроэнтерол. 1999;94:2135–2140. [PubMed] [Google Scholar]
61. Delhaye M, Vandermeeren A, Baize M, Cremer M. Экстракорпоральная ударно-волновая литотрипсия камней поджелудочной железы. Гастроэнтерология. 1992; 102: 610–620. [PubMed] [Google Scholar]
62. Dumonceau JM, Costamagna G, Tringali A, Vahedi K, Delhaye M, Hittelet A, Spera G, Giostra E, Mutignani M, De Maertelaer V, et al. Лечение болезненного кальцифицированного хронического панкреатита: экстракорпоральная ударно-волновая литотрипсия в сравнении с эндоскопическим лечением: рандомизированное контролируемое исследование. Кишка. 2007; 56: 545–552. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Cremer M, Devière J, Delhaye M, Baize M, Vandermeeren A. Стентирование при тяжелом хроническом панкреатите: результаты среднесрочного наблюдения за 76 пациентами. Эндоскопия. 1991; 23: 171–176. [PubMed] [Google Scholar]
Эндоскопия. 1991; 23: 171–176. [PubMed] [Google Scholar]
64. Grimm H, Meyer WH, Nam VC, Soehendra N. Новые методы лечения хронического панкреатита. Эндоскопия. 1989; 21: 70–74. [PubMed] [Google Scholar]
65. Perwaiz A, Singh A, Chaudhary A. Хирургия хронического панкреатита. Индийский Дж. Сург. 2012;74:47–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Клименко А.В., Клименко В.Н., Стешенко А.А., Туманский В.А., Коваленко И.С. Клинико-морфологические обоснования выполнения паренхимосохраняющих операций в хирургии хронического панкреатита // Клин. 2012;(1):14–18. [PubMed] [Google Scholar]
67. Strobel O, Büchler MW, Werner J. Хирургическое лечение хронического панкреатита: показания, методы и результаты. Int J Surg. 2009;7:305–312. [PubMed] [Google Scholar]
68. Fisher AV, Sutton JM, Wilson GC, Hanseman DJ, Abbott DE, Smith MT, Schmulewitz N, Choe KA, Wang J, Sussman JJ, et al. Высокая частота повторных госпитализаций после операций по поводу хронического панкреатита. Операция. 2014; 156:787–794. [PubMed] [Google Scholar]
Операция. 2014; 156:787–794. [PubMed] [Google Scholar]
69. Ян С.Дж., Блисс Л.А., Шапира Э.Ф., Фридман С.Д., Нг С.К., Виндзор Дж.А., Ценг Дж.Ф. Систематический обзор ранней хирургии хронического панкреатита: влияние на боль, функцию поджелудочной железы и повторное вмешательство. J Gastrointest Surg. 2014; 18:1863–1869. [PubMed] [Google Scholar]
70. Bouwense SA, Ahmed Ali U, ten Broek RP, Issa Y, van Eijck CH, Wilder-Smith OH, van Goor H. Изменение центральной обработки боли после операции на поджелудочной железе при хроническом панкреатите. Бр Дж Сур. 2013;100:1797–1804. [PubMed] [Google Scholar]
71. Fried M, Schwizer W, Beglinger C, Keller U, Jansen JB, Lamers CB. Физиологическая роль холецистокинина в постпрандиальной секреции инсулина и опорожнении желудка у человека. Исследования с антагонистом холецистокининовых рецепторов локсиглумидом. Диабетология. 1991; 34: 721–726. [PubMed] [Google Scholar]
72. Keller J, Layer P. Экзокринная реакция поджелудочной железы человека на питательные вещества в норме и при болезни. Кишка. 2005; 54 Приложение 6: vi1–28. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Кишка. 2005; 54 Приложение 6: vi1–28. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Грин Г.М., Лайман Р.Л. Обратная регуляция секреции ферментов поджелудочной железы как механизм гиперсекреции, вызванной ингибитором трипсина, у крыс. Proc Soc Exp Biol Med. 1972; 140: 6–12. [PubMed] [Google Scholar]
74. Ihse I, Lilja P, Lundquist I. Трипсин как регулятор секреции поджелудочной железы у крыс. Scand J Гастроэнтерол. 1979; 14: 873–880. [PubMed] [Google Scholar]
75. Louie DS, May D, Miller P, Owyang C. Холецистокинин опосредует обратную регуляцию секреции ферментов поджелудочной железы у крыс. Am J Physiol. 1986;250:G252–G259. [PubMed] [Google Scholar]
76. Rausch U, Weidenbach H, Adler G, Kern HF. Стимуляция секреторного процесса поджелудочной железы у крыс низкомолекулярным ингибитором протеиназ. II. Регуляция биосинтеза общего белка и отдельных ферментов. Сотовые Ткани Res. 1987; 249: 63–67. [PubMed] [Google Scholar]
77. Ширатори К., Чен Ю. Ф., Чей В.И., Ли К.И., Чанг Т.М. Механизм увеличения экзокринной секреции поджелудочной железы у крыс с отведением панкреатического сока. Гастроэнтерология. 1986;91:1171–1178. [PubMed] [Google Scholar]
Ф., Чей В.И., Ли К.И., Чанг Т.М. Механизм увеличения экзокринной секреции поджелудочной железы у крыс с отведением панкреатического сока. Гастроэнтерология. 1986;91:1171–1178. [PubMed] [Google Scholar]
78. Черник С.С., Лепковский С., Чайков И.Л. Диетический фактор, регулирующий содержание ферментов поджелудочной железы; изменения, вызванные размером и протеолитической активностью поджелудочной железы цыплят при употреблении в пищу сырой соевой муки. Am J Physiol. 1948; 155: 33–41. [PubMed] [Google Scholar]
79. Корринг Т. Механизм экзокринной секреции поджелудочной железы у свиньи. Регулирование обратной связи. Энн Биол Амин Биохим Биофиз. 1973; 13: 755–756. [Академия Google]
80. Louie DS, Williams JA, Owyang C. Действие полипептида поджелудочной железы на секрецию поджелудочной железы крыс: in vivo и in vitro. Am J Physiol. 1985; 249:G489–G495. [PubMed] [Google Scholar]
81. Petersen H, Grossman MI. Экзокринная секреция поджелудочной железы у наркотизированных и находящихся в сознании крыс. Am J Physiol. 1977; 233:E530–E536. [PubMed] [Google Scholar]
Am J Physiol. 1977; 233:E530–E536. [PubMed] [Google Scholar]
82. Герац Д.Д. Секреторная стимуляция поджелудочной железы крыс п-аминобензамидином. Am J Physiol. 1969; 216: 812–817. [PubMed] [Академия Google]
83. Гератц Д.Д., Хёрт Д.П. Регуляция уровня ферментов поджелудочной железы ингибиторами трипсина. Am J Physiol. 1970; 219: 705–711. [PubMed] [Google Scholar]
84. Fukuoka S, Kawajiri H, Fushiki T, Takahashi K, Iwai K. Локализация секреционно-стимулирующей активности ферментов поджелудочной железы и ингибирующей активности трипсина в гранулах зимогена поджелудочной железы крысы. Биохим Биофиз Акта. 1986; 884: 18–24. [PubMed] [Google Scholar]
85. Lu L, Louie D, Owyang C. Высвобождающий холецистокинин пептид опосредует обратную регуляцию секреции поджелудочной железы. Am J Physiol. 1989;256:G430–G435. [PubMed] [Google Scholar]
86. Миясака К., Green GM. Влияние атропина на базальную секрецию поджелудочной железы крыс при возврате или отведении желчно-панкреатического сока. Proc Soc Exp Biol Med. 1983; 174: 187–192. [PubMed] [Google Scholar]
Proc Soc Exp Biol Med. 1983; 174: 187–192. [PubMed] [Google Scholar]
87. Noda A, Magee DF, Sarles H. Роль желудочной секреции в гиперсекреции поджелудочной железы после отклонения у крыс в сознании. Дж. Физиол. 1982; 326: 453–459. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Owyang C, Louie DS, Tatum D. Обратная регуляция секреции ферментов поджелудочной железы. Подавление высвобождения холецистокинина трипсином. Джей Клин Инвест. 1986;77:2042–2047. [Бесплатная статья PMC] [PubMed] [Google Scholar]
89. Owyang C, May D, Louie DS. Трипсин угнетает секрецию ферментов поджелудочной железы. Дифференциальное влияние на выброс холецистокинина и энтеропанкреатический рефлекс. Гастроэнтерология. 1986; 91: 637–643. [PubMed] [Google Scholar]
90. Ихсе И. Лечение боли при хроническом панкреатите ферментами поджелудочной железы. Ферменты поджелудочной железы в норме и при патологии. В: Lankisch PG, редактор. Берлин: Springer-Verlag; 1991. С. 89–94. [Академия Google]
91. Фолш УР. Лечение боли при хроническом панкреатите ферментами поджелудочной железы. Противоположная позиция. Ферменты поджелудочной железы в норме и при патологии. В: Lankisch PG, редактор. Берлин: Springer-Verlag; 1991. С. 97–102. [Google Scholar]
Фолш УР. Лечение боли при хроническом панкреатите ферментами поджелудочной железы. Противоположная позиция. Ферменты поджелудочной железы в норме и при патологии. В: Lankisch PG, редактор. Берлин: Springer-Verlag; 1991. С. 97–102. [Google Scholar]
92. Ihse I, Lilja P, Lundquist I. Регулирование по обратной связи секреции панкреатических ферментов кишечным трипсином у человека. пищеварение. 1977; 15: 303–308. [PubMed] [Google Scholar]
93. Ясуи А., Нимура Ю., Хаякава Н., Хаякава Т., Сибата Т., Кондо Т., Нарусэ С., Шионоя С. Регуляция базальной секреции поджелудочной железы по обратной связи у людей. Поджелудочная железа. 1988;3:681–687. [PubMed] [Google Scholar]
94. Slaff J, Jacobson D, Tillman CR, Curington C, Toskes P. Протеазоспецифическое подавление экзокринной секреции поджелудочной железы. Гастроэнтерология. 1984; 87: 44–52. [PubMed] [Google Scholar]
95. Burton FR, Garvin PJ, Joshi SN. Экзокринная супрессия фистулы трансплантата поджелудочной железы человека пероральными ферментами поджелудочной железы. Трансплантация. 1989; 47: 888–891. [PubMed] [Google Scholar]
Трансплантация. 1989; 47: 888–891. [PubMed] [Google Scholar]
96. Бертон Ф.Р., Бертон М.С., Гарвин П.Дж., Джоши С.Н. Ингибирование экзокринной секреции трансплантированной поджелудочной железы человека по принципу обратной связи с энтеральными ферментами поджелудочной железы. Трансплантация. 1992;54:988–992. [PubMed] [Google Scholar]
97. Liener IE, Goodale RL, Deshmukh A, Satterberg TL, Ward G, DiPietro CM, Bankey PE, Borner JW. Влияние ингибитора трипсина из соевых бобов (Bowman-Birk) на секреторную активность поджелудочной железы человека. Гастроэнтерология. 1988; 94: 419–427. [PubMed] [Google Scholar]
98. Adler G, Müllenhoff A, Koop I, Bozkurt T, Göke B, Beglinger C, Arnold R. Стимуляция секреции поджелудочной железы у человека ингибитором протеазы (камостатом) Eur J Clin Invest. 1988;18:98–104. [PubMed] [Google Scholar]
99. Adler G, Müllenhoff A, Bozkurt T, Göke B, Koop I, Arnold R. Сравнение влияния однократного и многократного введения ингибитора протеазы (камостата) на секрецию поджелудочной железы у человека. . Scand J Гастроэнтерол. 1988; 23: 158–162. [PubMed] [Google Scholar]
. Scand J Гастроэнтерол. 1988; 23: 158–162. [PubMed] [Google Scholar]
100. Krawisz BR, Miller LJ, DiMagno EP, Go VL. В отсутствие питательных веществ секреция панкреатических желчевыводящих путей в тощей кишке не оказывает обратной связи на функцию поджелудочной железы или желудка человека. J Lab Clin Med. 1980;95:13–18. [PubMed] [Google Scholar]
101. Hotz J, Ho SB, Go VL, DiMagno EP. Кратковременное ингибирование активности трипсина в двенадцатиперстной кишке не влияет на функцию поджелудочной железы, желчевыводящих путей или желудка. J Lab Clin Med. 1983; 101: 488–495. [PubMed] [Google Scholar]
102. Dlugosz J, Fölsch UR, Creutzfeldt W. Ингибирование интрадуоденального трипсина не стимулирует экзокринную секрецию поджелудочной железы у человека. пищеварение. 1983; 26: 197–204. [PubMed] [Google Scholar]
103. Bastedo WA. Использование и полезность пищеварительных ферментов в терапии: резюме ответов на вопросник, представленный членам Американской гастроэнтерологической ассоциации. ДЖАМА. 1925;85:743–744. [Google Scholar]
ДЖАМА. 1925;85:743–744. [Google Scholar]
104. Райт Дж.С. Индианаполис: Эли Лилли и компания; 1895. Справочник по органическим лекарствам Объединенной государственной фармакопеи 1890; п. 93. [Google Scholar]
105. Транг Т., Чан Дж., Грэм Д.Ю. Заместительная ферментная терапия панкреатической внешнесекреторной недостаточности в 21 веке. Мир J Гастроэнтерол. 2014;20:11467–11485. [Бесплатная статья PMC] [PubMed] [Google Scholar]
106. Браун А., Хьюз М., Теннер С., Бэнкс П.А. Уменьшают ли добавки ферментов поджелудочной железы боль у пациентов с хроническим панкреатитом: метаанализ. Am J Гастроэнтерол. 1997;92:2032–2035. [PubMed] [Google Scholar]
107. Шафик Н., Рана С., Бхасин Д., Панди П., Шривастава П., Семби С.С., Кумар Р., Малхотра С. Ферменты поджелудочной железы при хроническом панкреатите. Cochrane Database Syst Rev. 2009;(4):CD006302. [PubMed] [Google Scholar]
108. Исакссон Г., Ихсе И. Уменьшение боли пероральным препаратом ферментов поджелудочной железы при хроническом панкреатите. Dig Dis Sci. 1983; 28: 97–102. [PubMed] [Google Scholar]
Dig Dis Sci. 1983; 28: 97–102. [PubMed] [Google Scholar]
109. Malesci A, Gaia E, Fioretta A, Bocchia P, Ciravegna G, Cantor P, Vantini I. Отсутствие эффекта длительного лечения экстрактом поджелудочной железы на рецидивирующую боль в животе у пациентов с хроническим панкреатит. Scand J Гастроэнтерол. 1995;30:392–398. [PubMed] [Google Scholar]
110. Halgreen H, Pedersen NT, Worning H. Симптоматический эффект терапии ферментами поджелудочной железы у пациентов с хроническим панкреатитом. Scand J Гастроэнтерол. 1986; 21: 104–108. [PubMed] [Google Scholar]
111. Mössner J, Secknus R, Meyer J, Niederau C, Adler G. Лечение боли экстрактами поджелудочной железы при хроническом панкреатите: результаты проспективного плацебо-контролируемого многоцентрового исследования. пищеварение. 1992; 53: 54–66. [PubMed] [Академия Google]
112. Ларвин М., МакМахон М.Дж., Томас В.Е.Г., Пунтис М.К.А. Креон (панкреатические микросферы, покрытые кишечнорастворимой оболочкой) для лечения боли при хроническом панкреатите. Двойное слепое рандомизированное плацебо-контролируемое перекрестное исследование. Гастроэнтерология. 1991;100:А283. [Google Scholar]
Двойное слепое рандомизированное плацебо-контролируемое перекрестное исследование. Гастроэнтерология. 1991;100:А283. [Google Scholar]
113. Сафди М., Бекал П.К., Мартин С., Саид З.А., Бертон Ф., Тоскес П.П. Влияние пероральных ферментов поджелудочной железы (капсула Creon 10) на стеаторею: многоцентровое плацебо-контролируемое исследование с параллельными группами у пациентов с хроническим панкреатитом. Поджелудочная железа. 2006; 33: 156–162. [PubMed] [Академия Google]
114. Lankisch PG, Lembcke B, Göke B, Creutzfeldt W. Терапия панкреатогенной стеатореи: дает ли какое-либо преимущество кислотная защита ферментов поджелудочной железы? Z Гастроэнтерол. 1986; 24: 753–757. [PubMed] [Google Scholar]
115. Домингес-Муньос Дж. Э., Иглесиас-Гарсия Дж., Иглесиас-Рей М., Фигейрас А., Вилариньо-Инсуа М. Влияние схемы приема на терапевтическую эффективность пероральных ферментных добавок поджелудочной железы у пациентов с экзокринной недостаточностью поджелудочной железы: рандомизированное трехстороннее перекрестное исследование. Алимент Фармакол Тер. 2005;21:993–1000. [PubMed] [Google Scholar]
Алимент Фармакол Тер. 2005;21:993–1000. [PubMed] [Google Scholar]
116. O’Keefe SJ, Cariem AK, Levy M. Обострение эндокринной дисфункции поджелудочной железы мощными экзокринными добавками поджелудочной железы у пациентов с хроническим панкреатитом. Дж. Клин Гастроэнтерол. 2001; 32: 319–323. [PubMed] [Google Scholar]
117. Winstead NS, Wilcox CM. Клинические испытания заместительной терапии ферментами поджелудочной железы при болезненном хроническом панкреатите — обзор. Панкреатология. 2009; 9: 344–350. [PubMed] [Google Scholar]
118. Czakó L, Takács T, Hegyi P, Prónai L, Tulassay Z, Lakner L, Döbrönte Z, Boda K, Lonovics J. Оценка качества жизни после заместительной терапии ферментами поджелудочной железы при хроническом панкреатите . Можно J Гастроэнтерол. 2003;17:597–603. [PubMed] [Google Scholar]
119. D’Haese JG, Ceyhan GO, Demir IE, Layer P, Uhl W, Löhr M, Rychlik R, Pirilis K, Zöllner Y, Gradl B, et al. Заместительная терапия ферментами поджелудочной железы у пациентов с экзокринной недостаточностью поджелудочной железы из-за хронического панкреатита: 1-летнее исследование контроля симптомов и качества жизни. Поджелудочная железа. 2014;43:834–841. [PubMed] [Google Scholar]
Поджелудочная железа. 2014;43:834–841. [PubMed] [Google Scholar]
120. Sikkens EC, Cahen DL, Koch AD, Braat H, Poley JW, Kuipers EJ, Bruno MJ. Распространенность дефицита жирорастворимых витаминов и снижение костной массы у больных хроническим панкреатитом. Панкреатология. 2013; 13: 238–242. [PubMed] [Академия Google]
121. Губергриц Н., Малецка-Панас Э., Леман Г.А., Васильева Г., Шен Ю., Сандер-Штракмайер С., Карас С., Уиткомб Д.С. 6-месячное открытое клиническое исследование капсул с отсроченным высвобождением панкрелипазы (Креон) у пациентов с внешнесекреторной недостаточностью поджелудочной железы вследствие хронического панкреатита или операции на поджелудочной железе. Алимент Фармакол Тер. 2011;33:1152–1161. [PubMed] [Google Scholar]
122. Taylor JR, Gardner TB, Waljee AK, Dimagno MJ, Schoenfeld PS. Систематический обзор: эффективность и безопасность добавок ферментов поджелудочной железы при экзокринной недостаточности поджелудочной железы. Алимент Фармакол Тер. 2010; 31:57–72. [PubMed] [Академия Google]
2010; 31:57–72. [PubMed] [Академия Google]
123. Деньги М.Е., Хофманн А.Ф., Хейги Л.Р., Валковяк Дж., Тэлли Н.Дж. Лечение синдрома раздраженного кишечника-диареи с помощью панкреалипазы или колесевелама и ассоциации со стеатореей. Поджелудочная железа. 2009; 38: 232–233. [PubMed] [Google Scholar]
124. Money ME, Walkowiak J, Virgilio C, Talley NJ. Пилотное исследование: рандомизированное, двойное слепое, плацебо-контролируемое исследование панкреалипазы для лечения постпрандиального синдрома раздраженного кишечника-диареи. Фронтлайн Гастроэнтерол. 2011;2:48–56. [Бесплатная статья PMC] [PubMed] [Google Scholar]
125. Money ME, Camilleri M. Review: Лечение синдрома постпрандиальной диареи. Am J Med. 2012; 125: 538–544. [PubMed] [Google Scholar]
126. Умнова Л., Орликов Г., Войцеховска Дж., Войцеховскис В., Крастинс Е. Комбинированное медикаментозное лечение хронического панкреатита. Proc Латвийской академии наук. 2016;2015:20–26. [Google Scholar]
127. Frieden TR, Houry D. Снижение рисков облегчения — руководство CDC по назначению опиоидов. N Engl J Med. 2016; 374:1501–1504. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Frieden TR, Houry D. Снижение рисков облегчения — руководство CDC по назначению опиоидов. N Engl J Med. 2016; 374:1501–1504. [Бесплатная статья PMC] [PubMed] [Google Scholar]
128. Deyo RA, Von Korff M, Duhrkoop D. Опиоиды при болях в пояснице. БМЖ. 2015;350:g6380. [Бесплатная статья PMC] [PubMed] [Google Scholar]
129. Braden JB, Young A, Sullivan MD, Walitt B, Lacroix AZ, Martin L. Предикторы изменения боли и физического функционирования у женщин в постменопаузе с рецидивирующей болью условия в обсервационной когорте Инициативы женского здоровья. Джей Пейн. 2012; 13:64–72. [Бесплатная статья PMC] [PubMed] [Google Scholar]
130. Wilder-Smith CH, Hill L, Osler W, O’Keefe S. Влияние трамадола и морфина на боль и моторную функцию желудочно-кишечного тракта у пациентов с хроническим панкреатитом. Dig Dis Sci. 1999;44:1107–1116. [PubMed] [Google Scholar]
131. Grunkemeier DM, Cassara JE, Dalton CB, Drossman DA. Синдром наркотического кишечника: клиника, патофизиология, лечение. Клин Гастроэнтерол Гепатол. 2007; 5:1126–1139. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Клин Гастроэнтерол Гепатол. 2007; 5:1126–1139. [Бесплатная статья PMC] [PubMed] [Google Scholar]
132. Тутея А.К., Бискупяк Дж., Стоддард Г.Дж., Липман А.Г. Опиоид-индуцированные расстройства кишечника и наркотический кишечный синдром у пациентов с хронической неонкологической болью. Нейрогастроэнтерол Мотил. 2010;22:424–430, e96. [PubMed] [Академия Google]
133. Szigethy E, Schwartz M, Drossman D. Синдром наркотического кишечника и запор, вызванный опиоидами. Curr Gastroenterol Rep. 2014; 16:410. [PubMed] [Google Scholar]
134. Дроссман Д., Сигети Э. Наркотический синдром кишечника: недавнее обновление. Am J Gastroenterol Suppl. 2014; 2:22–30. [PubMed] [Google Scholar]
135. Грэм Д.Ю. Нестероидные противовоспалительные препараты, Helicobacter pylori и язвы: наша позиция. Am J Гастроэнтерол. 1996;91:2080–2086. [PubMed] [Академия Google]
136. Olesen SS, Bouwense SA, Wilder-Smith OH, van Goor H, Drewes AM. Прегабалин уменьшает боль у пациентов с хроническим панкреатитом в рандомизированном контролируемом исследовании. Гастроэнтерология. 2011; 141: 536–543. [PubMed] [Google Scholar]
Гастроэнтерология. 2011; 141: 536–543. [PubMed] [Google Scholar]
Сроки возобновления питания после острого панкреатита
by Simone Gärtner
Добавить в закладки/Искать это сообщение
Симона Гертнер, Антье Стивелинг и Питер Саймон
Медицинский университет Грайфсвальда, медицинский факультет A, Ferdinand-Sauerbruch-Straße
17475 Greifswald, Germany
Версия заявки:
Версия 1.0, 19 августа 2016 г.
Ссылка:
Резюме 9 0294
Начальное лечение острого панкреатита в основном поддерживающее и состоит режима ничего не перорально вместе с внутривенной инфузионной реанимацией и анальгезией. Несмотря на то, что при остром панкреатите часто встречается дефицит питательных веществ, долгое время считалось, что нутритивная терапия — перорально или через зонд — оказывает негативное влияние на прогрессирование заболевания. Было опубликовано несколько исследований для определения оптимального времени, графика и типа перорального питания при остром панкреатите. Они показывают, что раннее возобновление питания с помощью твердой диеты безопасно и может сократить продолжительность пребывания в больнице. Не было обнаружено повышенного риска непереносимости повторного питания, рецидива заболевания или других нежелательных явлений, связанных с более активным протоколом возобновления питания. При легком и тяжелом остром панкреатите в Руководстве ESPEN рекомендуются активные попытки орального питания после устранения выходной обструкции желудка и контроля осложнений. В зависимости от клинического течения питание может быть изменено на облегченную полноценную диету, и нет особой необходимости в пошаговом переходе на нормальную полноценную диету согласно данным Немецкого общества нутрициологии в сотрудничестве со швейцарским, австрийским и немецким обществами в их S3-Руководство.
Было опубликовано несколько исследований для определения оптимального времени, графика и типа перорального питания при остром панкреатите. Они показывают, что раннее возобновление питания с помощью твердой диеты безопасно и может сократить продолжительность пребывания в больнице. Не было обнаружено повышенного риска непереносимости повторного питания, рецидива заболевания или других нежелательных явлений, связанных с более активным протоколом возобновления питания. При легком и тяжелом остром панкреатите в Руководстве ESPEN рекомендуются активные попытки орального питания после устранения выходной обструкции желудка и контроля осложнений. В зависимости от клинического течения питание может быть изменено на облегченную полноценную диету, и нет особой необходимости в пошаговом переходе на нормальную полноценную диету согласно данным Немецкого общества нутрициологии в сотрудничестве со швейцарским, австрийским и немецким обществами в их S3-Руководство.
1. Введение
В начале острого панкреатита происходит ранняя активация пищеварительных ферментов с последующей системной воспалительной реакцией, опосредованной цитокинами. Лечение зависит от степени тяжести (9).
Лечение зависит от степени тяжести (9).
Несмотря на то, что при остром панкреатите часто встречается дефицит питания, долгое время считалось, что нутритивная терапия — перорально или через зонд — оказывает негативное влияние на исход заболевания из-за предполагаемой стимуляции экзокринной секреции поджелудочной железы и последующего ухудшения состояния. аутопищеварительные процессы в поджелудочной железе (17). Цель голодания как традиционной терапии острого панкреатита заключалась в том, чтобы «успокоить поджелудочную железу». Большая часть этого убеждения основана на физиологических исследованиях и не подтверждается данными проспективных клинических испытаний.
Мета-анализ клинических исследований показал, что при остром панкреатите энтеральное питание превосходит парентеральное с точки зрения сопутствующих осложнений и стоимости. Энтеральное питание имеет преимущество в плане снижения риска инфекционных осложнений и смертности (5, 15, 16, 22, 24). Мета-анализы показывают, что при остром панкреатите наблюдались значительно более низкие показатели смертности, когда энтеральное питание начинали в течение 24 часов после госпитализации, по сравнению с введением в период от 24 до 72 часов (14). преимущество раннего начала повторного кормления (2).
преимущество раннего начала повторного кормления (2).
При легком остром панкреатите традиционное лечение по-прежнему включает начальное голодание в течение 2 или 3 дней. С этого момента пероральное питание постепенно увеличивают от прозрачных жидкостей до мягкой твердой пищи, а выписку из стационара планируют на основе переносимости пациентом твердой пищи (25). Исследования оптимального времени и диеты для перорального питания при остром панкреатите все еще редки.
2. Когда начинать пероральное питание
Пациенты с легким острым панкреатитом обычно не имеют повышенных потребностей в питательных веществах или энергии (17). У этих пациентов энтеральное питание не требуется, если через 5-7 дней пациент может употреблять обычную пищу перорально. Энтеральное питание в течение 5-7 дней не оказывает положительного влияния на течение заболевания и поэтому не рекомендуется (17).
При легком и тяжелом остром панкреатите в Руководстве ESPEN по энтеральному питанию рекомендуются активные попытки перорального питания (обычной пищей и/или пищевыми добавками) после устранения выходной обструкции желудка, учитывая, что это не вызывает боли, а осложнения возможны. под контролем. Таким образом, кормление через зонд можно постепенно сокращать по мере улучшения перорального питания (17).
под контролем. Таким образом, кормление через зонд можно постепенно сокращать по мере улучшения перорального питания (17).
Различные подходы к выбору времени нормального приема пищи через рот после острого панкреатита изучались в клинических исследованиях. Проспективное исследование Levy et al. показали, что пациенты могут принимать пищу перорально после короткого периода голодания, если боль прекратилась, а уровни амилазы и липазы снижаются (13). Рецидив боли после возобновления кормления через рот наблюдался у 21% пациентов в первый и второй день возобновления питания (4). Повышение липазы в три раза по сравнению с верхней границей нормы и более высокая оценка по шкале Бальхазара в начале возобновления кормления были идентифицированы как факторы риска рецидив боли (13, 23).
Тейх и др. исследовали оптимальные сроки возобновления перорального питания при легком остром панкреатите (25). Они сравнили самостоятельно отобранную группу, в которой пациентам разрешалось возобновлять прием пищи по своему выбору, и группу, в которой пациенты получали липазу, в которой пациентам не разрешалось есть до тех пор, пока значение липазы не упадет ниже значения, в 2 раза превышающего верхний предел референтного диапазона. . Они показали, что самостоятельно выбранная группа не превосходила группу, получавшую липазу, но также не создавала дополнительного риска по сравнению с традиционным голоданием. Они также показали тенденцию к более короткому пребыванию в стационаре в группе самостоятельных повторных кормлений и отсутствию обострения боли или более высокой частоте рецидивов (25).
. Они показали, что самостоятельно выбранная группа не превосходила группу, получавшую липазу, но также не создавала дополнительного риска по сравнению с традиционным голоданием. Они также показали тенденцию к более короткому пребыванию в стационаре в группе самостоятельных повторных кормлений и отсутствию обострения боли или более высокой частоте рецидивов (25).
В исследовании Li аналогичным образом проанализированы две группы пациентов с легким острым панкреатитом (14). Одни начинали есть, как только чувствовали голод, а другие начинали есть, когда выполняли следующие критерии: 1) отсутствие болей в животе; 2) снижение уровня амилазы и липазы в сыворотке менее чем в 2 раза по сравнению с верхней границей референтного диапазона; 3) нормальные кишечные шумы; 4) субъективное чувство голода. Не было различий в частоте рецидивов болей в животе, активности сывороточной амилазы или липазы переходного вздутия живота выше верхней границы нормы или гипергликемии после перорального питания между этими группами (14). Это исследование свидетельствует о том, что лучшее время для возобновления перорального питания — это когда пациент чувствует голод, и этот подход безопасен и сокращает продолжительность пребывания в больнице. Нет необходимости откладывать пероральное кормление до тех пор, пока не исчезнут боли в животе или не нормализуются ферменты поджелудочной железы в сыворотке.
Это исследование свидетельствует о том, что лучшее время для возобновления перорального питания — это когда пациент чувствует голод, и этот подход безопасен и сокращает продолжительность пребывания в больнице. Нет необходимости откладывать пероральное кормление до тех пор, пока не исчезнут боли в животе или не нормализуются ферменты поджелудочной железы в сыворотке.
Тот же вопрос исследовался у больных с острым панкреатитом средней и тяжелой степени. Среднетяжелый или тяжелый острый панкреатит часто вызывает осложнения и приводит к высокому катаболическому, гиперметаболическому и гипердинамическому стрессу с более высокой заболеваемостью и смертностью. Оптимальная нутритивная поддержка стала ключевым элементом в лечении этих пациентов. Данные о возобновлении перорального питания при умеренном или тяжелом панкреатите в основном отсутствуют. В исследовании Li et al. показали эквивалентные результаты для повторного кормления на основе чувства голода при умеренном и тяжелом панкреатите (14). Чжао и др. показали, что повторное кормление, основанное на чувстве голода, безопасно. Хотя это увеличивает риск гипергликемии, который может быть сведен к минимуму строгим протоколом контроля уровня глюкозы, между двумя группами не было различий в отношении боли в животе, рецидива вздутия живота, органной недостаточности или возникновения местных или системных осложнений до выписки. из больницы (27).
Чжао и др. показали, что повторное кормление, основанное на чувстве голода, безопасно. Хотя это увеличивает риск гипергликемии, который может быть сведен к минимуму строгим протоколом контроля уровня глюкозы, между двумя группами не было различий в отношении боли в животе, рецидива вздутия живота, органной недостаточности или возникновения местных или системных осложнений до выписки. из больницы (27).
Эккерволл и др. продемонстрировали в клиническом рандомизированном исследовании эффективность и осуществимость немедленного перорального питания ad libitum по сравнению с традиционным голоданием и поэтапным возобновлением перорального приема пищи у пациентов с легким острым панкреатитом (6). Они показали, что пациенты с немедленным пероральным питанием раньше начинали с твердой пищи и нуждались в меньшем количестве дней внутривенного введения жидкости. Признаков обострения болезненного процесса, усиления болей в животе или ряда желудочно-кишечных симптомов в результате немедленного перорального питания не было. Они также показали связь со значительным сокращением продолжительности пребывания в больнице с 6 до 4 дней по сравнению с группой натощак (6).
Они также показали связь со значительным сокращением продолжительности пребывания в больнице с 6 до 4 дней по сравнению с группой натощак (6).
Лариньо-Нойя и др. аналогичным образом было обнаружено, что раннее возобновление питания, как только появились кишечные шумы, сокращает продолжительность пребывания в больнице на два дня по сравнению со стандартным протоколом возобновления питания (12).
3. Тип состава для перорального питания
В типичном протоколе перорального повторного питания диета вводится постепенно, начиная с небольшого количества прозрачных жидкостей в течение первых 24 часов. При хорошей переносимости диету постепенно меняют на мягкую, с низким содержанием жиров, за которой следует твердая диета. В этом случае выписка из больницы зависит от переносимости твердой диеты с низким содержанием жиров (26).
Исследование Jacobson et al. исследовали начало перорального питания в течение 3 дней после госпитализации с использованием прозрачной жидкой диеты (588 ккал, 2 г жира) или твердой диеты с низким содержанием жира (1200 ккал, 35 г жира) у пациентов после легкого острого панкреатита. Они не обнаружили существенной разницы в доле пациентов, не переносящих пероральное кормление, что позволяет предположить, что обе практики безопасны (10).
Они не обнаружили существенной разницы в доле пациентов, не переносящих пероральное кормление, что позволяет предположить, что обе практики безопасны (10).
Стандартное повторное кормление со ступенчатым увеличением потребления калорий не требуется, как показано Lariño-Noia et al. (12). Было показано, что раннее повторное кормление с использованием диеты с низким содержанием жира 1800 ккал с первого дня, как только появились шумы в кишечнике, хорошо переносятся и безопасны. Желудочно-кишечные жалобы были зарегистрированы без существенных отличий от группы стандартного возобновления питания (12). Сходные результаты были получены между гипокалорийной прозрачной жидкой диетой, промежуточной гипокалорийной мягкой диетой и полной твердой диетой у пациентов с легким острым панкреатитом. Не было различий в частоте рецидивов боли или продолжительности пребывания в стационаре (18, 20).
Поэтому Немецкое общество медицины питания в сотрудничестве с Обществом клинического питания Швейцарии, Австрийским консорциумом клинического питания и Немецким обществом гастроэнтерологов в своем Руководстве S3 рекомендует, чтобы в зависимости от клинического течения питание можно было изменить на легкая полноценная диета (21). Особой необходимости в ступенчатом переходе на обычный полноценный рацион нет. Признаки клинически значимой мальабсорбции в течение тяжелого острого панкреатита могут привести к замещению ферментов поджелудочной железы (21). Рекомендуется пероральное возобновление питания с помощью диеты, богатой углеводами и белками и с низким содержанием жиров (<30% от общего потребления энергии), но ни одно клиническое исследование не показало его превосходства над другими составами пищи. Если диета хорошо переносится, пероральное питание можно постоянно увеличивать, и специальные продукты не требуются (17).
Особой необходимости в ступенчатом переходе на обычный полноценный рацион нет. Признаки клинически значимой мальабсорбции в течение тяжелого острого панкреатита могут привести к замещению ферментов поджелудочной железы (21). Рекомендуется пероральное возобновление питания с помощью диеты, богатой углеводами и белками и с низким содержанием жиров (<30% от общего потребления энергии), но ни одно клиническое исследование не показало его превосходства над другими составами пищи. Если диета хорошо переносится, пероральное питание можно постоянно увеличивать, и специальные продукты не требуются (17).
4. Ферментные добавки при раннем пероральном возобновлении питания
Экзокринная недостаточность поджелудочной железы является актуальной проблемой после острого панкреатита. Тяжесть внешнесекреторной недостаточности напрямую связана с тяжестью заболевания (3, 7, 8, 19). Даже у больных с легким острым панкреатитом внешнесекреторная функция нарушена в начале острого приступа, но у большинства больных восстанавливается (7). У некоторых из этих пациентов возникают абдоминальные симптомы во время перорального кормления (например, метеоризм, диарея и боль). Это может быть связано с экзокринной недостаточностью поджелудочной железы в момент начала возобновления питания (11). Эффект раннего введения ферментов поджелудочной железы в период возобновления питания после острого панкреатита оценивался Kahl и соавт. (11). Они показали тенденцию к более быстрому восстановлению экзокринной недостаточности поджелудочной железы при добавлении ферментов по сравнению с плацебо (14 дней против 23 дней; p = 0,641) и отсутствие значимых различий в отношении безопасности и переносимости. Эйри и др. также продемонстрировали значительное улучшение экзокринной функции поджелудочной железы после пяти дней повторного кормления добавками ферментов поджелудочной железы (1).
У некоторых из этих пациентов возникают абдоминальные симптомы во время перорального кормления (например, метеоризм, диарея и боль). Это может быть связано с экзокринной недостаточностью поджелудочной железы в момент начала возобновления питания (11). Эффект раннего введения ферментов поджелудочной железы в период возобновления питания после острого панкреатита оценивался Kahl и соавт. (11). Они показали тенденцию к более быстрому восстановлению экзокринной недостаточности поджелудочной железы при добавлении ферментов по сравнению с плацебо (14 дней против 23 дней; p = 0,641) и отсутствие значимых различий в отношении безопасности и переносимости. Эйри и др. также продемонстрировали значительное улучшение экзокринной функции поджелудочной железы после пяти дней повторного кормления добавками ферментов поджелудочной железы (1).
5. Заключение
Было проведено небольшое количество исследований с целью определения оптимальных сроков, схемы и типа перорального питания при остром панкреатите.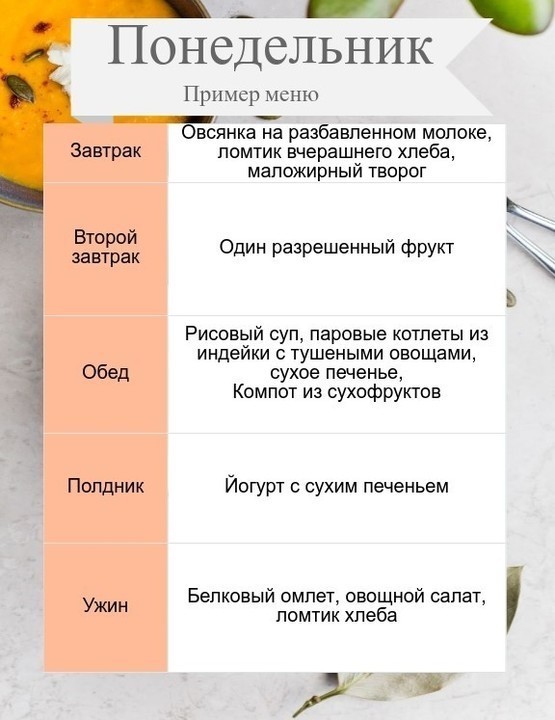 Они показывают, что нормализация уровня ферментов поджелудочной железы не является предварительным условием для начала перорального питания. Позволить пациенту выбирать, когда возобновить пероральное питание, независимо от уровня ферментов в сыворотке, может быть наиболее подходящим вариантом. Кроме того, раннее возобновление питания может сократить продолжительность пребывания в больнице. До сих пор нет единого мнения об определении «раннего возобновления кормления».
Они показывают, что нормализация уровня ферментов поджелудочной железы не является предварительным условием для начала перорального питания. Позволить пациенту выбирать, когда возобновить пероральное питание, независимо от уровня ферментов в сыворотке, может быть наиболее подходящим вариантом. Кроме того, раннее возобновление питания может сократить продолжительность пребывания в больнице. До сих пор нет единого мнения об определении «раннего возобновления кормления».
Пероральный прием обычно начинается с прозрачных жидкостей, за которыми следует твердая пища с низким содержанием жира с увеличением калорийности в течение 3-6 дней, по-видимому, не имеет преимуществ перед началом с обычной легкой пищи. Таким образом, раннее пероральное возобновление питания с помощью твердой диеты может обеспечить лучшие результаты и безопасно для пациентов с легким и умеренным острым панкреатитом. Тем не менее, лучшее рандомизированное исследование не смогло показать преимущества раннего повторного кормления по сравнению с повторным кормлением по требованию пациентов (2), когда пациенты чувствуют себя готовыми принимать обычную пищу через рот. Ни в одном из ранее опубликованных исследований не наблюдалось повышенного риска непереносимости повторного кормления или других нежелательных явлений, связанных с более активным протоколом возобновления питания. Несколько исследований показывают, что прием ферментов поджелудочной железы в начале перорального возобновления питания может быть полезным с точки зрения предотвращения рецидивов боли, но для подтверждения этой потенциальной пользы необходимы дальнейшие исследования.
Ни в одном из ранее опубликованных исследований не наблюдалось повышенного риска непереносимости повторного кормления или других нежелательных явлений, связанных с более активным протоколом возобновления питания. Несколько исследований показывают, что прием ферментов поджелудочной железы в начале перорального возобновления питания может быть полезным с точки зрения предотвращения рецидивов боли, но для подтверждения этой потенциальной пользы необходимы дальнейшие исследования.
6. Ссылки
- Airey MC и McMahon MJ . Ферменты поджелудочной железы в норме и болезни. Берлин, Гейдельберг, Springer Berlin Heidelberg, 1991.
- Bakker OJ, van Brunschot S, van Santvoort HC, Besselink MG, Bollen TL, Boermeester MA, et al. Раннее кормление через назоэнтеральный зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med 371(21): 1983-1993, 2014. PMID: 25409371.
- Бюхлер М.
 , Хауке А. и Малфертхайнер А. . Последующее наблюдение после острого панкреатита: Морфология и функция. Острый панкреатит . Г. Г. Бегер и М. В. Бюхлер. Берлин, Гейдельберг, Springer Verlag : 367–374, 1987.
, Хауке А. и Малфертхайнер А. . Последующее наблюдение после острого панкреатита: Морфология и функция. Острый панкреатит . Г. Г. Бегер и М. В. Бюхлер. Берлин, Гейдельберг, Springer Verlag : 367–374, 1987. - Chebli JM, Gaburri PD, De Souza AF, Junior EV, Gaburri AK, Felga GE, et al. Пероральное возобновление питания у пациентов с легким острым панкреатитом: распространенность и факторы риска рецидивирующей боли в животе. J Гастроэнтерол Гепатол 20(9): 1385-1389, 2005. PMID: 16105125.
- Дервенис С . Энтеральное питание при тяжелом остром панкреатите: перспективы развития. JOP 5(2): 60-63, 2004. PMID: 15007186.
- Eckerwall GE, Tingstedt BB, Bergenzaun PE и Andersson RG . Немедленное пероральное питание у пациентов с легким острым панкреатитом безопасно и может ускорить выздоровление — рандомизированное клиническое исследование. Clin Nutr 26(6): 758-763, 2007.
 PMID: 17719703.
PMID: 17719703. - Гласбреннер Б., Бюхлер М., Уль В. и Малфертхайнер П. . Внешнесекреторная функция поджелудочной железы в ранний восстановительный период острого отечного панкреатита. J Gastroenterol Hepatol 4: 563–567, 1992.
- Гулло Л, Сарлес Х и Мотт CB . Функциональное исследование экзокринной части поджелудочной железы после острого панкреатита. Rendiconti di Gastroenterologia 4: 18-21, 1972.
- Халангк В. и Лерх М.М. . Ранние проявления острого панкреатита. Gastroenterol Clin North Am 33(4): 717-731, 2004. PMID: 15528014.
- Джейкобсон Б.К., Вандер Влит М.Б., Хьюз М.Д., Маурер Р., Макманус К. и Бэнкс П.А. . Проспективное рандомизированное исследование прозрачных жидкостей по сравнению с твердой диетой с низким содержанием жира в качестве первого приема пищи при легком остром панкреатите. Clin Gastroenterol Hepatol 5(8): 946-951; викторина 886,2007.
 PMID: 17613280.
PMID: 17613280. - Каль С., Шютте К., Гласбреннер Б., Майерле Дж., Саймон П., Хеннигес Ф. и др. Влияние пероральных добавок ферментов поджелудочной железы на течение и исход острого панкреатита: рандомизированное двойное слепое исследование в параллельных группах. JOP 15(2): 165-174, 2014. PMID: 24618443.
- Ларино-Нойя Дж., Линдквист Б., Иглесиас-Гарсия Дж., Сейхо-Риос С., Иглесиас-Канле Дж. и Домингес-Муньос Дж. Э. . Раннее и/или немедленное полнокалорийное питание по сравнению со стандартным возобновлением питания при легком остром панкреатите: рандомизированное открытое исследование. Панкреатология 14(3): 167-173, 2014. PMID: 24854611.
- Леви П., Хересбах Д., Парьенте Э.А., Борухович А., Дельсенсери Р., Миллат Б. и др. Частота и факторы риска рецидивирующей боли во время возобновления питания у пациентов с острым панкреатитом: многофакторное многоцентровое проспективное исследование 116 пациентов.
 Gut 40(2): 262-266, 1997. PMID: 9071942.
Gut 40(2): 262-266, 1997. PMID: 9071942. - Ли Х, Ма Ф и Цзя К . Раннее энтеральное питание в течение 24 часов или между 24 и 72 часами при остром панкреатите: доказательства, основанные на 12 РКИ. Med Sci Monit 20: 2327-2335, 2014. PMID: 25399541.
- Марик ЧП и Залога ГП . Метаанализ парентерального питания по сравнению с энтеральным питанием у пациентов с острым панкреатитом. БМЖ 328 (7453): 1407, 2004. PMID: 15175229.
- Макклэйв С.А., Чанг В.К., Даливал Р. и Хейланд Д.К. . Нутритивная поддержка при остром панкреатите: систематический обзор литературы. J Parenter Enteral Nutr 30(2): 143-156, 2006. PMID: 16517959.
- Мейер Р., Окенга Дж., Перткевич М., Пап А., Милиник Н., Макфи Дж. и др. Руководство ESPEN по энтеральному питанию: Поджелудочная железа. Clin Nutr 25(2): 275-284, 2006. PMID: 16678943.
- Meng WB, Li X, Li YM, Zhou WC и Zhu XL .
 Три начальные диеты для лечения легкого острого панкреатита: метаанализ. World J Gastroenterol 17(37): 4235-4241, 2011. PMID: 22072857.
Три начальные диеты для лечения легкого острого панкреатита: метаанализ. World J Gastroenterol 17(37): 4235-4241, 2011. PMID: 22072857. - Migliori M, Pezzilli R, Tomassetti P и Gullo L . Внешнесекреторная функция поджелудочной железы после алкогольного или билиарного острого панкреатита. Поджелудочная железа 28(4): 359-363, 2004. PMID: 15097850.
- Moraes JM, Felga GE, Chebli LA, Franco MB, Gomes CA, Gaburri PD, et al. Полноценная твердая диета в качестве первого приема пищи при легком остром панкреатите безопасна и приводит к сокращению продолжительности госпитализации: результаты проспективного, рандомизированного, контролируемого, двойного слепого клинического исследования. J Clin Gastroenterol 44(7): 517-522, 2010. PMID: 20054282.
- Окенга Дж., Лёзер К., Крафт М. и Мадл К. . S3-Leitlinie der Deutschen Gesellschaft für Ernährungsmedizin e . В . Klinische Ernährung in der Gastroenterologie (Teil 3).
 Aktuelle Ernährungsmedizin 39(57): 7143–7156, 2014.
Aktuelle Ernährungsmedizin 39(57): 7143–7156, 2014. - Петров М.С., Пилипчук Р.Д. и Емельянов Н.В. . Систематический обзор: нутритивная поддержка при остром панкреатите. Aliment Pharmacol Ther 28(6): 704-712, 2008. PMID: 19145726.
- Петров М.С., ван Сантвоорт Х.К., Бесселинк М.Г., Циркель Г.А., Бринк М.А. и Гузен Х.Г. . Пероральное возобновление питания после начала острого панкреатита: обзор литературы. Am J Gastroenterol 102(9): 2079-2084; викторина 2085,2007. PMID: 17573797.
- Петров М.С., ван Сантвоорт Х.К., Бесселинк М.Г., ван дер Хейден Г.Дж., Виндзор Дж.А. и Гусен Х.Г. . Энтеральное питание и риск смертности и инфекционных осложнений у больных тяжелым острым панкреатитом: метаанализ рандомизированных исследований. Arch Surg 143(11): 1111-1117,2008. PMID: 1
71.
- Teich N, Aghdassi A, Fischer J, Walz B, Caca K, Wallochny T, et al. Оптимальные сроки возобновления перорального питания при легком остром панкреатите: результаты открытого рандомизированного многоцентрового исследования.






 Травяной чай
Травяной чай
 Удалению конкрементов может способствовать лазерная или контактная литотрипсия в сочетании со сфинктеротомией и эндоскопической экстракцией разрушенных конкрементов.
Удалению конкрементов может способствовать лазерная или контактная литотрипсия в сочетании со сфинктеротомией и эндоскопической экстракцией разрушенных конкрементов.
 Может быть выполнена холецистэктомия (как традиционая, так и лапароскопическая) с дренированием общего желчного протока, или наложен билиодигестивный анастомоз (сформировано сообщение между желчным протоком и кишкой -двенадцатиперстной или тощей), выполнена папиллосфинктеротомия(рассечение рубцово суженого большого дуоденального соска) или папиллосфинктеропластика.
Может быть выполнена холецистэктомия (как традиционая, так и лапароскопическая) с дренированием общего желчного протока, или наложен билиодигестивный анастомоз (сформировано сообщение между желчным протоком и кишкой -двенадцатиперстной или тощей), выполнена папиллосфинктеротомия(рассечение рубцово суженого большого дуоденального соска) или папиллосфинктеропластика. Они направлены на купирование боли и снижение функции поджелудочной железы.
Они направлены на купирование боли и снижение функции поджелудочной железы.  , Хауке А. и Малфертхайнер А. . Последующее наблюдение после острого панкреатита: Морфология и функция. Острый панкреатит . Г. Г. Бегер и М. В. Бюхлер. Берлин, Гейдельберг, Springer Verlag : 367–374, 1987.
, Хауке А. и Малфертхайнер А. . Последующее наблюдение после острого панкреатита: Морфология и функция. Острый панкреатит . Г. Г. Бегер и М. В. Бюхлер. Берлин, Гейдельберг, Springer Verlag : 367–374, 1987. PMID: 17719703.
PMID: 17719703.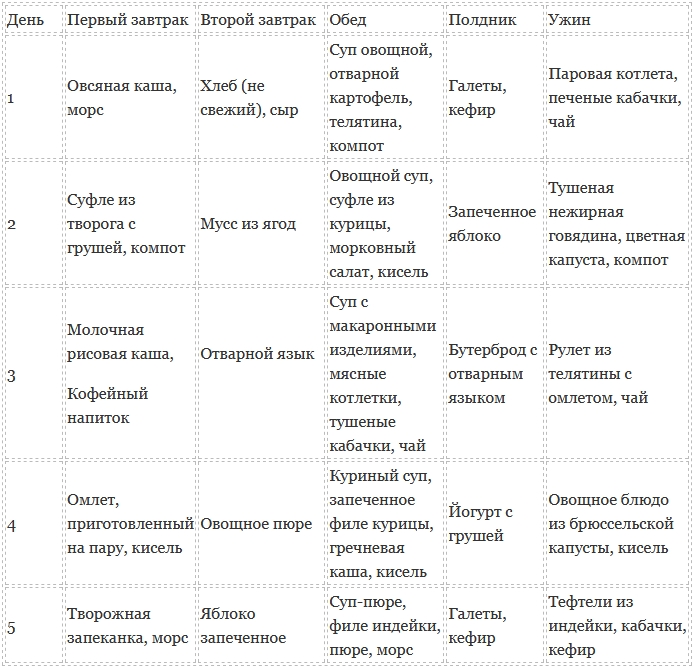 PMID: 17613280.
PMID: 17613280. Gut 40(2): 262-266, 1997. PMID: 9071942.
Gut 40(2): 262-266, 1997. PMID: 9071942. Три начальные диеты для лечения легкого острого панкреатита: метаанализ. World J Gastroenterol 17(37): 4235-4241, 2011. PMID: 22072857.
Три начальные диеты для лечения легкого острого панкреатита: метаанализ. World J Gastroenterol 17(37): 4235-4241, 2011. PMID: 22072857.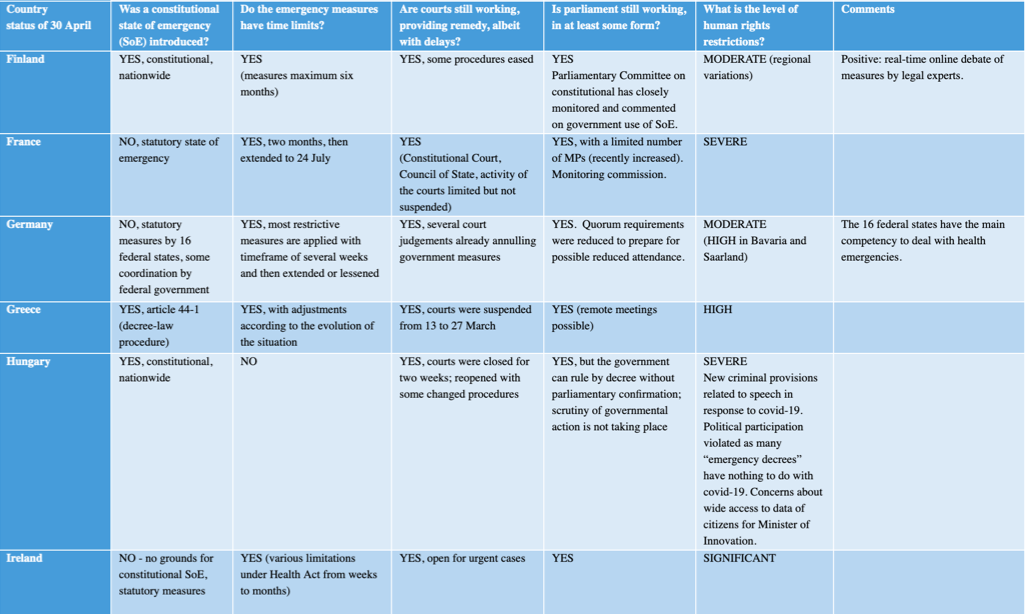 Aktuelle Ernährungsmedizin 39(57): 7143–7156, 2014.
Aktuelle Ernährungsmedizin 39(57): 7143–7156, 2014.